
(12��)��1���ڻ�ѧ��Ӧ�У�ֻ�м�����������ƽ�������ߵö�ķ�Ӧ����ӷ�����ײʱ�ſ��ܷ�����ѧ��Ӧ����Щ���ӳ�Ϊ����ӣ�ʹ��ͨ���ӱ�ɻ���������ṩ������ȵ������л�ܣ��䵥λͨ����kJ/mol��ʾ��������۲���ͼ��Ȼ��ش����⣺
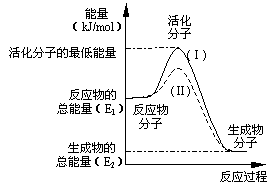 ��ͼ����ʾ��Ӧ��_____________������ȡ�
��ͼ����ʾ��Ӧ��_____________������ȡ�
���ȡ�����Ӧ���÷�Ӧ____________
�����Ҫ������Ҫ�������ȣ��÷�Ӧ��
��H��____________���ú�E1��E2�Ĵ���ʽ��ʾ����
����֪�Ȼ�ѧ����ʽ��H2(g)��1/2O2(g)��H2O(g)��
��H����241.8 kJ/mol���÷�Ӧ�Ļ��Ϊ
167.2kJ/mol�������淴Ӧ�Ļ��Ϊ____________��
�۶���ͬһ��Ӧ��ͼ�����ߣ�����ʵ�ߣ�����ȣ�
��ܴ�ͣ�����ӵİٷ������࣬��Ӧ�������Լӿ죬����Ϊ����ܵ�ԭ����_________ ____________________________________________��
��2�����ſ�ѧ�����Ľ��������������˶��ּ״����ӽ���Ĥȼ�ϵ�أ������㲻ͬ������
����һ��״����ӽ���Ĥȼ�ϵ�أ��轫�״�����ת��Ϊ���������ַ�Ӧԭ����
A��CH3OH(g)��H2O(g)��CO2(g)��3H2(g) ��H����49.0kJ/mol
B��CH3OH(g)��3/2O2(g)��CO2(g)��2H2O(g) ��H����192.9kJ/mol
��֪H2O(l)= H2O(g) ��H����44 kJ/mol����д��32g��CH3OH(g)��ȫȼ������Һ̬ˮ���Ȼ�ѧ����ʽ ��
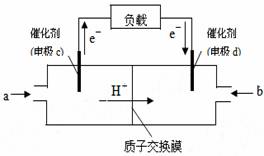 ����ͼ��ij�ʼDZ������ü״����ӽ���Ĥȼ�ϵ�صĽṹʾ��ͼ��
����ͼ��ij�ʼDZ������ü״����ӽ���Ĥȼ�ϵ�صĽṹʾ��ͼ��
�״��ڴ����������ṩ���Ӻ͵��ӣ����Ӿ����·��
���Ӿ��ڵ�·������һ����������Ӧ������ܷ�ӦΪ��
2CH3OH��3O2��2CO2��4H2O����c�缫��
�������������������c�缫�Ϸ����ĵ缫��Ӧʽ
�� ��
 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ��ʼ����ʱ��pH | ������ȫʱ��pH | |
| Mg2+ | 9.6 | 11.0 |
| Ca2+ | 12.2 | c��OH-��=1.8mol?L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��09��10�꽨�����и߶���ѧ����ĩ���Ի�ѧ�� ���ͣ������
������12�֣�
A��п��һ����Ҫ�Ľ�����п���仯�������Ź㷺��Ӧ�á�
��1����������п[CH2OH��CHOH4COO��2Zn��Ŀǰ�г������еIJ�п����д��Zn2+��
̬�����Ų�ʽ ��������[CH2OH��CHOH��4CHO]������̼ԭ���ӻ���ʽ�� ��
��2��Zn2+Ҳ����NH3�γ�������[Zn��NH3��4]2+����λ��NH3���ӿռ乹��Ϊ ��
��[Zn��NH3��4]2+�У�Zn2+λ�������������ģ�Nλ����������Ķ��㣬������ͼ��
��ʾ[Zn��NH3��4]2+��Zn2+��N֮��Ļ�ѧ�� ��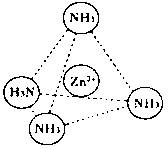
��3����ͼ��ʾп��ij��Ԫ��X�γɵĻ����ᄃ��������Zn��Xͨ�����ۼ���ϣ��û�����Ļ�ѧʽΪ ��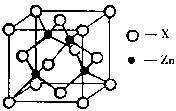
�û�����ľ����۵�ȸɱ��ߵö࣬ԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012�갲������13У�߶���ѧ�������������ƻ�ѧ�Ծ����������� ���ͣ������
(12��)�����ϣ�ҩѧ�ң��й���ҽ�о�Ժ�����о�Ա����ϯ�о�Ա���������о������������Ρ����������ҩ������ҩ����о���ͻ�������Ǵ������Ϳ�űҩ�����������غ�˫�������ء�2011��9�£���ñ���Ϊŵ������������ꡱ����˹�˽��������й�����ҽѧ������Ϊֹ��õ����缶�����
��֪��������ṹ��ʽ��ͼһ��Ҳ�ɱ�ʾΪͼ������ʽ����Ű��ҩ�����صĽṹ��ʽ��ͼ����ʾ�����й���������O��O��������ǿ�����ԣ�������ɱ����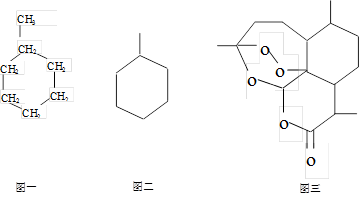
������ѧ֪ʶ�ش��й����⣺
��1��д�������صķ���ʽ ��
��2�������й������ص�������ȷ���ǣ� ��
A.�������Ƿ����庬�������� B.�����ؾ���ǿ�����ԣ�������ɱ��
C.���������ڷ��ࡢ���������� D.1mol������ˮ������2molNaOH
��3���˹��ϳ������صĹؼ�����������Ȼ���ȩΪԭ�ϣ����������������⡣�����л��ϳ��������ǻ��ķ�Ӧ�����У� ��
��ȡ�� �ڼӳ� ����ȥ ������ �ݻ�ԭ
A.�ڢ� B.�٢ڢ� C.�٢� D. �٢ڢۢ�
��4��һ����Ȼ���ȩ�Ľṹ��ʽΪ�� ���йط�Ӧ�������£�
���йط�Ӧ�������£�
�ٲ���٢۵������� ��
��д���������ʵĽṹ��ʽA B ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012���Ϻ����ֶ�����������ѧ��4��������⻯ѧ�Ծ����������� ���ͣ������
�����12�֣��Ե����ᣨF���Ľṹ��ʽΪ�� �����Ǵ���������ֲ���е�һ�ֶ�ӣ����п��������ӻ�˥�ϡ����ʽ�֬�ȹ�Ч����AΪԭ�Ϻϳ�F��·�����£�
�����Ǵ���������ֲ���е�һ�ֶ�ӣ����п��������ӻ�˥�ϡ����ʽ�֬�ȹ�Ч����AΪԭ�Ϻϳ�F��·�����£�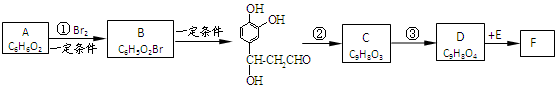
��������ش��������⣺
1��д���ṹ��ʽ��A____________��D___________________��
2��д����Ӧ���ͣ���Ӧ��________����Ӧ��______________��
3����Ӧ�۵��Լ���____________________________________��
4�� 1 mol F�ֱ�����������ˮ��NaOH��Һ��Ӧ����������Br2_____mol��NaOH____mol��
5��E��һ�������·������۷�Ӧ�Ļ�ѧ����ʽ�ǣ���֪�������ǻ�����ֱ�������ᷢ��������Ӧ��______________________________________________________________��
6����E��Ϊͬ���칹�壬��ͬʱ���������������л�����_____________�֡�
�ٱ��������ĸ�ȡ�������ұ����ϵ�һ��ȡ����ֻ��һ�֡�
��1 mol�����ʷֱ���NaHCO3��Na2CO3��Ӧʱ���������NaHCO3��Na2CO3�����ֱ���1 mol��4 mol��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com