
一定条件下,可逆反应的平衡常数可以用平衡浓度计算, 也可以用平衡分压代替平衡浓度计算,分压=总压×物质的量分数。在恒温恒压条件下,总压不变,用平衡分压计算平衡常数更方便。下列说法不正确的是
也可以用平衡分压代替平衡浓度计算,分压=总压×物质的量分数。在恒温恒压条件下,总压不变,用平衡分压计算平衡常数更方便。下列说法不正确的是
A.对于C2H4(g)+H2O(g)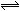 C2H5OH(g)在一定条件下达到平衡状态时,体系的总压强为P,其中C2H4(g)、H2O(g)、C2H5OH(g)均为1 mol,则用分压表示的平衡常数KP=3/P
C2H5OH(g)在一定条件下达到平衡状态时,体系的总压强为P,其中C2H4(g)、H2O(g)、C2H5OH(g)均为1 mol,则用分压表示的平衡常数KP=3/P
B.恒温恒压下,在一容积可变的容器中,反应2A(g)+B(g)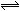 2C(g)达到平衡时,A、B和C的物质的量分别为4 mol、 2 mol和4 mol.若此时A、B和C均增加1 mol,平衡正向移动
2C(g)达到平衡时,A、B和C的物质的量分别为4 mol、 2 mol和4 mol.若此时A、B和C均增加1 mol,平衡正向移动
C.恒温恒压下,在一容积可变的容器中,N2(g)+3H2(g)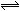 2NH3(g)达到平衡状态时,N2、H2、NH3各1 mol,若此时再充入3 mol N2,则平衡正向移动
2NH3(g)达到平衡状态时,N2、H2、NH3各1 mol,若此时再充入3 mol N2,则平衡正向移动
D.对于一定条件下的某一可逆反应,用平衡浓度表示的平衡常数和用平衡分压表示的平衡常数,其数值不同,但意义相同,都只与温度有关
科目:高中化学 来源:2016-2017学年黑龙江大庆铁人中学高一阶段考一化学卷(解析版) 题型:选择题
下列实验操作中错误的是( )
A. 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
B. 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C. 蒸馏中,冷却水应从冷凝管的下口通入,上口流出
D. 过滤操作时,漏斗颈下端不能紧靠烧杯内壁
查看答案和解析>>
科目:高中化学 来源:2016-2017年黑龙江哈尔滨师大附中高一10月月考化学卷(解析版) 题型:选择题
配制一定体积一定浓度的NaOH溶液时,下列操作导致结果偏高的是
A.称量NaOH固体时动作缓慢 B.定容时俯视刻度线
C.定容后振荡发现液面低于刻度线 D.未洗涤烧杯和玻璃棒
查看答案和解析>>
科目:高中化学 来源:2016-2017年黑龙江哈尔滨师大附中高一10月月考化学卷(解析版) 题型:选择题
下列有关实验的叙述正确的是
A. 用酒精萃取溴水中的溴单质的操作可选用分液漏斗,而后静置分液
B. 蒸馏时,温度计的水银球应靠近蒸馏烧瓶的底部
C. 容量瓶用水洗净后,可不经干燥直接用于配制溶液
D. 配制1L0.1mol/L的NaCl溶液时可用托盘天平称量5.85gNaCl固体
查看答案和解析>>
科目:高中化学 来源:2016-2017年黑龙江哈尔滨师大附中高二10月月考化学卷(解析版) 题型:填空题
在恒温容器中加入1 mol N2和3 mol H2,达到平衡时NH3的体积分数为m%。若N2、H2、NH3的起始加入量分别为x mol、y mol、z mol,达到平衡时NH3的体积分数仍为m%。
(1)该容器恒容,则x、 y、z应满足的关系是 。
y、z应满足的关系是 。
(2)该容器恒压,则x、y、z应满足的关系是 。
(3)若该容器恒压,前者达到平衡时生成NH3为a moL,则后者达到平衡时生成NH3 mol(用a、x、z表示)。
查看答案和解析>>
科目:高中化学 来源:2016-2017年黑龙江哈尔滨师大附中高二10月月考化学卷(解析版) 题型:选择题
一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如下图所示:
下列描述正确的是
A.反应开始到10 s,用Z表示的反应速率为0.158 mol•L-1•s-1
B.反应开始到10 s,X的物质的量浓度为减少了0.79 mol•L-1
C.反应开始到10 s时,Y的转化率为79.0%
D.反应的化学方程式为:X(g) + Y(g)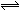 Z(g)
Z(g)
查看答案和解析>>
科目:高中化学 来源:2016-2017年黑龙江哈尔滨师大附中高二10月月考化学卷(解析版) 题型:选择题
下列有关活化分子和活化能的说法不正确的是
A.增加气体反应物的浓度可以提高活化分子百分数
B.升高温度可增加单位体积活化分子数
C.发生有效碰撞的分子一定是活化分子
D.使用催化剂可降低活化能,提高活化分子百分数
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上10月月考化学卷(解析版) 题型:选择题
已知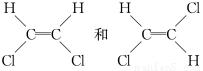 互为同分异构体,则化学式为C3H5Cl的有机物的同分异构体共有 ( )
互为同分异构体,则化学式为C3H5Cl的有机物的同分异构体共有 ( )
A.3种 B.4种 C.5种 D.6种
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上10月月考化学试卷(解析版) 题型:选择题
下列常用的混合物分离或提纯操作中,需使用分液漏斗的是( )
A.过滤 B.蒸发 C.蒸馏 D.分液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com