
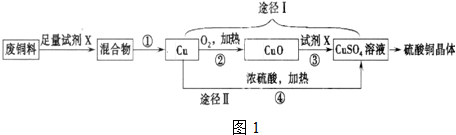

分析 加入的X需将铁除去,且不能与铜反应选择稀硫酸,反应①为铁与硫酸反应生成硫酸亚铁和氢气,化学方程式为Fe+H2SO4 ═FeSO4+H2↑,过滤后铜与氧气反应②为:2Cu+O2 $\frac{\underline{\;\;△\;\;}}{\;}$2CuO,转化为氧化铜,反应③CuO+H2SO4═CuSO4+H2O;途径Ⅱ,在加热条件下,Cu和浓硫酸发生氧化还原反应生成CuSO4、SO2、H2O,反应方程式为Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
(1)加入的X需将铁除去,且不能与铜反应选择稀硫酸,固液分离用过滤操作;
(2)途径Ⅰ:2Cu+O2 $\frac{\underline{\;\;△\;\;}}{\;}$2CuO,转化为氧化铜,CuO+H2SO4═CuSO4+H2O没有二氧化硫产生,硫酸的利用率高,无污染;
(3)①A装置为分液漏斗,在该装置中滴加浓硫酸;
②若要收集满干燥的SO2气体,装置排列顺序为:气体发生装置、干燥装置、收集装置、检验装置、尾气处理装置;
解答 解:(1)废铜料中有铁和铜,要生产硫酸铜,需将铁除去,因此可加入足量稀硫酸将铁除去,铜与硫酸不反应,过滤后得到固体铜,
故答案为:H2SO4;过滤;
(2)途径Ⅱ是铜与浓硫酸反应Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O生成硫酸铜、二氧化硫和水,二氧化硫为有毒气体,且浪费硫酸,因此对比途径I、Ⅱ,途径Ⅰ没有二氧化硫产生,硫酸的利用率高,无污染,
故答案为:ad;
(3)①装置A、a,用浓硫酸与铜反应制取二氧化硫,装置A为分液漏斗,用于滴加浓硫酸,
故答案为:分液漏斗;
②制取干燥的SO2气体,装置排列顺序为:气体发生装置、干燥装置、收集装置、检验装置、尾气处理装置,A、a 为气体发生装置、b、c(f、g)为收集装置、d、e用浓硫酸是干燥装置、f、g(b、c)是防倒吸装置、h是尾气处理装置,所以排列顺序是debcgfh或defgbch,
故答案为:debcgf或defgbc;
点评 本题考查硫酸铜、二氧化硫的制备,侧重考查学生实验操作、分析能力,会根据实验目的排列装置顺序,易错选项是(3)③,注意酸性条件下硝酸根离子的性质、硫元素的化合价变化,题目难度中等.


 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
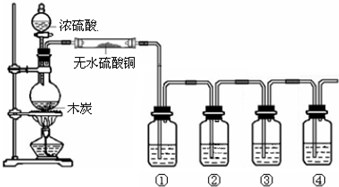
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
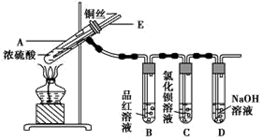
| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 | BaSO4 | BaSO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
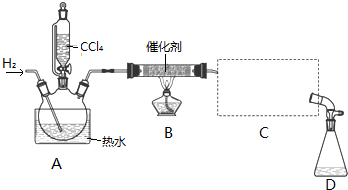
| 物质 | 相对分子质量 | 密度/(g•mL-1) | 沸点/℃ | 水中溶解性 |
| CHCl3 | 119.5 | 1.50 | 61.3 | 难溶 |
| CCl4 | 154 | 1.59 | 76.7 | 难溶 |
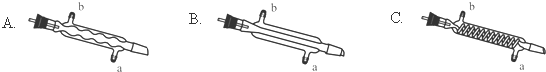
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
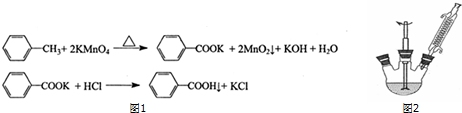
| 名称 | 相对分子质量 | 性状 | 熔点/℃ | 溶解度 | |
| 水 | 乙醇 | ||||
| 甲苯 | 92 | 无色液体易烯易挥发 | -95 | 不溶 | 易溶 |
| 苯甲酸 | 122 | 白色片状或针状晶体 | 122.4(100℃升华) | 25℃0.35g 80℃2.7g | 易溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
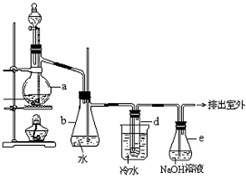 醇与氢卤酸反应是制备卤代烃的重要方法.实验室制备溴乙烷的装置如下图所示,试管d中装有少量蒸馏水.已知溴乙烷的沸点为38.4oC,密度为1.43g•ml-1;
醇与氢卤酸反应是制备卤代烃的重要方法.实验室制备溴乙烷的装置如下图所示,试管d中装有少量蒸馏水.已知溴乙烷的沸点为38.4oC,密度为1.43g•ml-1;查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com