
| A、利用催化设施,可以将汽车尾气中CO和NO转化为无害气体 |
| B、在入海口的钢闸门上装一定数量的铜块可防止闸门被腐蚀 |
| C、先通入氯气,再加入硫酸亚铁处理水,能达到消毒杀菌和除去悬浮杂质的目的 |
| D、半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是硅 |


科目:高中化学 来源: 题型:
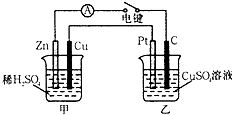 (Ⅰ)某兴趣小组的同学用下图所示装置研究有关电化学的问题.当闭合该装置的电键时,观察到电流计的指针发生了偏转.请回答下列问题:
(Ⅰ)某兴趣小组的同学用下图所示装置研究有关电化学的问题.当闭合该装置的电键时,观察到电流计的指针发生了偏转.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、C+O2
| ||||
B、CaCO3
| ||||
C、2KMnO4
| ||||
| D、Zn+H2SO4=ZnSO4+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素Y的最高正化合价为+6 |
| B、离子半径的大小顺序为W>Q>Z>X>Y |
| C、氢化物的沸点Y>W |
| D、元素W的最高价氧化物对应水化物的酸性比Q的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、①④ | C、②③ | D、③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 将镉(Cd)浸在氯化钴(CoCl2)溶液中,发生反应的离子方程式为:Co2+(aq)+Cd(s)=Co(s)+Cd2+(aq)(aq表示溶液),如将该反应设计为如右图的原电池,则下列说法一定错误的是( )
将镉(Cd)浸在氯化钴(CoCl2)溶液中,发生反应的离子方程式为:Co2+(aq)+Cd(s)=Co(s)+Cd2+(aq)(aq表示溶液),如将该反应设计为如右图的原电池,则下列说法一定错误的是( )| A、Cd作负极,Co作正极 |
| B、原电池工作时,电子从负极沿导线流向正极 |
| C、根据阴阳相吸原理,盐桥中的阳离子向负极(甲池)移 动 |
| D、甲池中盛放的是CdCl2溶液,乙池中盛放的是CoCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:

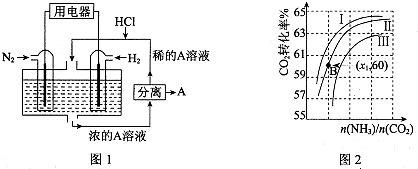
| n(NH3) |
| n(CO2) |
| n(H2O) |
| n(CO2) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com