
25℃时,2a mol·L-1HA水溶液中(HA为弱酸)。用NaOH调节溶液pH(忽略体积变化),得到c(HA)、c(A-)与溶液pH的变化关系如下图所示。下列说法错误的是
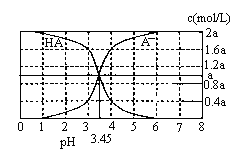
A.当pH=3时,溶液中c(A-)>c(Na+)
B.当c(A-)>c(HA),溶液一定呈碱性
C.当pH=3.45时,c(Na+)+c(H+)=c(HA)+c(OH-)
D.当pH=4时,溶液中:c(HA)+c(Na+)+c(H+)-c(OH-)=2a mol·L-1
B
【解析】
试题分析:A、当pH=3时,c(OH-)< c(H+)且溶液中存在电荷守恒:c(OH-)+c(A-)=c(Na+) +c(H+),所以溶液中c(A-)>c(Na+),正确;B、根据图像pH>3.45时,c(A-)>c(HA),溶液不一定呈碱性,错误;C、当pH=3.45时,c(A-)=c(HA)且c(OH-)+c(A-)=c(Na+) +c(H+),可得c(Na+)+c(H+)=c(HA)+c(OH-),正确;D、c(Na+)+c(H+)-c(OH-)=c(A-)=1.6a mol·L-1,c(HA)=0.4a mol·L-1,所以c(HA)+c(Na+)+c(H+)-c(OH-)=2a mol·L-1,正确。
考点:考查图像分析、溶液中离子浓度关系。


 星级口算天天练系列答案
星级口算天天练系列答案科目:高中化学 来源: 题型:
密闭容器中X、Y、Z三种气体的初始浓度和不同温度下的平衡浓度如下表:
|
查看答案和解析>>
科目:高中化学 来源: 题型:
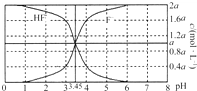 25℃时,2a mol?L-1氢氟酸水溶液中,用NaOH溶液调节溶液pH(忽略体积变化),得到c(HF)、c(F-)与溶液pH的变化关系如图所示.下列说法正确的是( )
25℃时,2a mol?L-1氢氟酸水溶液中,用NaOH溶液调节溶液pH(忽略体积变化),得到c(HF)、c(F-)与溶液pH的变化关系如图所示.下列说法正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
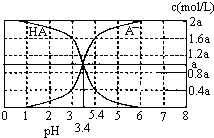 25℃时,2a mol?L-1HA水溶液中(HA为弱酸).用NaOH调节溶液pH(忽略体积变化),得到c(HA)、c(A-)与溶液pH的变化关系如下图所示.下列说法错误的是( )
25℃时,2a mol?L-1HA水溶液中(HA为弱酸).用NaOH调节溶液pH(忽略体积变化),得到c(HA)、c(A-)与溶液pH的变化关系如下图所示.下列说法错误的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
25℃时,2a mol·L—1HA水溶液中(HA为弱酸)。用NaOH调节溶液pH(忽略体积变化),得到c(HA)、c(A—)与溶液pH的变化关系如下图所示。下列说法错误的是
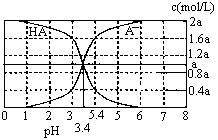
A.当pH=3时,溶液中c(A—)>c(Na+)
B.当c(A—)>c(HA),溶液一定呈碱性
C.当pH=3.45时,c(Na+)+c(H+)=c(HA)+c(OH—)
D.当pH=4时,溶液中:c(HA)+c(Na+)+c(H+)—c(OH—)=2a mol·L—1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com