
粒子结构示意图
粒子的核电荷数“+Z”加圈“○”,然后分层写出电子数。如:
Na________ Na+________ S________ S2-________
 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
-工业生产硫酸时,其中—步反应是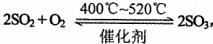 ,该反应正反应是放热反应。如果在密闭容器中进行反应,下列说法错误的是
,该反应正反应是放热反应。如果在密闭容器中进行反应,下列说法错误的是
A.升高温度可提高反应速率 B.使用催化剂能增大反应速率
C.增大氧气浓度可提高SO2的转化率 D.达到化学平衡时SO2的浓度与SO3的浓度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
某含有少量 FeCl2杂质的 FeCl3样品,现要测定其中铁元素的含量.实验步骤如下:
① 准确称量mg 样品;
② 向样品中加人 10 mL 5 mol · L一1的盐酸,再加人蒸馏水,配制成 250 mL 溶液; ③ 量取 25 mL 操作 ② 中配得的溶液,加人 3 mL 溴水,加热使之完全反应;
④ 趁热迅速加人质量分数为 10 %的氨水至过量,充分搅拌,使之完全沉淀;
⑤ 过滤,将沉淀洗涤后反复灼烧、冷却、称量至恒重。
请根据上面的叙述回答:
(1)溶解样品时要加人盐酸,其目的是_______________________________________
(2)配制 250 mL 溶液时,除需玻璃棒、烧杯外,还须用到的玻璃仪器是_________________________________________________
(3)加人溴水时发生反应的离子方程式是:
____________________________________________________
(4)若坩埚质量为 W1 g ,增锅与灼烧后固体的总质量是 W2 g ,则样品中铁元素的质量分数是_____________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,对于密闭容器中进行的可逆反应A(g)+3B(g) 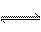 2C(g),下列说法中,能说明这一反应已经达到化学平衡状态的是( )
2C(g),下列说法中,能说明这一反应已经达到化学平衡状态的是( )
A.生成C的速率与C分解的速率相等 B.A、B、C的浓度相等
C.单位时间生成 n mol A,同时生成 3n mol B D.A、B、C的分子数之比为 1∶3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
离子化合物——左写原子的电子式(相同原子不可合并,因为要标出电子转移情况),用弯箭号标出电子转移情况,右写离子化合物的电子式,中间用“―→”连接即可。如:
MgCl2____________________________________________________________________
Na2S_____________________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
大气平流层中O2吸收紫外线可变成臭氧(O3),而冰箱中的制冷剂氟里昂在紫外线作用下分解出氯原子,氯原子能加速臭氧的分解,从而破坏平流层中的臭氧层。同样超音速飞机的尾气及发动机尾气中的NO也能加快O3的 分解,反应式如下:NO+O3===NO2+2O;NO2+O===NO+O2。请你写出总的反应式: ______________;其中NO的作用是______________和____________。
分解,反应式如下:NO+O3===NO2+2O;NO2+O===NO+O2。请你写出总的反应式: ______________;其中NO的作用是______________和____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
写出下列反应的化学方程式,并注明反应类型。(有机物用结构简式表示)
(1)由异戊二烯制备聚异戊二烯
反应类型:
(2)用甲苯制TNT 反应类型:
(3)实验室制取乙烯 反应类型:
(4)丙烯与溴化氢反应 反应类型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com