
如下图所示,将两烧杯中电极用导线相连,四个电极分别为Mg、Al、Pt、C。当闭合开关S后,以下表述正确的是( )
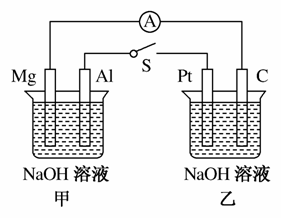
A.电流表指针不发生偏转
B.Al、Pt两极有H2产生
C.甲池pH增大,乙池pH减小
D.Mg、C两极生成的气体在一定条件下可以恰好完全反应
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
《课程标准(2011年版)》与《课程标准(实验稿)》相比,新增的二级主题是( )
A.认识几种化学反应 B.完成基础的学生实验
C.物质组成的表示 D.保护好我们的环境
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述不正确的是( )
A.原子间先通过得失电子变成阴、阳离子后,阴、阳离子间才能形成离子键
B.具有强得电子能力的原子与具有强失电子能力的原子相遇时能形成离子键
C.非金属原子间不可能形成离子键
D.含有金属元素的化合物不一定是离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
氮化钠(Na3N)是科学家制备的一种重要的化合物,它与水作用可产生NH3。请回答下列问题。
(1)Na3N的电子式是________,该化合物是由________键形成。
(2)Na3N与盐酸反应生成________种盐,其各种盐的电子式分别是______________________________________________________。
(3)Na3N与水的反应属于________反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
将a、b、c、d 4种金属两两连接浸入电解质溶液中,组成4个原电池(如图):
①中a极发生氧化反应 ②中电流由b到c ③中c极质量增加 ④中a极有大量气泡,则4种金属的活泼性由强到弱的顺序为( )
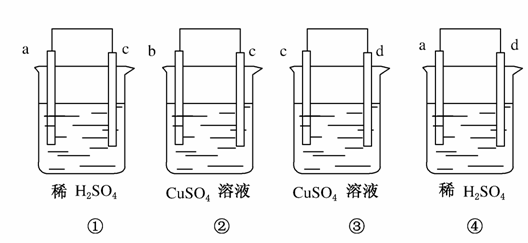
A.d>a>c>b B.d>c>a>b
C.b>d>c>a D.a>d>b>c
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室中的药品常按物质的性质、类别等有规律地摆放。现有部分药品按某种规律摆放在实验桌上,如下图。做实验时,某同学取用硝酸溶液后,应把它放回的位置是( )
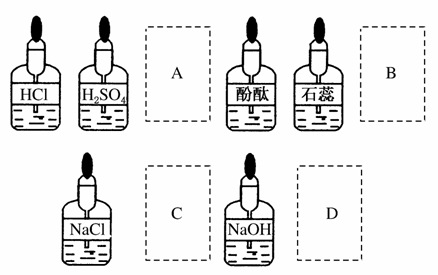
查看答案和解析>>
科目:高中化学 来源: 题型:
下列三组物质中,均有一种物质的类别与其他三种不同。
①MgO、Na2O、CO2、CuO ②HCl、H2O、H2SO4、HNO3 ③NaOH、Na2CO3、KOH、Cu(OH)2
(1)三种物质依次是(填化学式):A________;B________;C________。
(2)这三种物质相互作用可生成一种新物质NaHCO3,该反应________(“是”或“不是”)氧化还原反应。
(3)写出物质C与足量稀硫酸反应的离子方程式________________________________________。
(4)HCO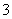 与H+、OH-在溶液中能共存吗?试用离子方程式说明____________________________________________________________________________________________________________________。
与H+、OH-在溶液中能共存吗?试用离子方程式说明____________________________________________________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com