
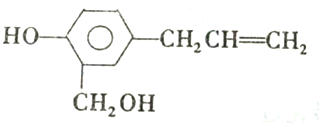
 对该物质的性质判断正确的是( )
对该物质的性质判断正确的是( )| A. | 等量A分别与Na和NaOH反应消耗二者的物质的量相同 | |
| B. | 1 mol A 可与2 mol Br2发生取代反应 | |
| C. | A与Na2CO3反应可放出CO2 | |
| D. | 1 mol A 可与4 mol H2发生反应 |
分析 该分子中含有酚羟基、醇羟基、苯环、碳碳双键,具有酚、醇、苯和烯烃性质,能发生取代反应、加成反应、酯化反应、氧化反应,据此分析解答.
解答 解:A.酚羟基和醇羟基都能和Na反应,只有酚羟基能和NaOH反应,所以等量A分别与Na和NaOH反应消耗二者的物质的量不相同,故A错误;
B.苯环上酚羟基邻对位氢原子能被溴原子取代,所以1 mol A 可与1mol Br2发生取代反应,故B错误;
C.酚羟基和碳酸钠反应生成碳酸氢钠和-ONa,没有二氧化碳生成,故C错误;
D.碳碳双键和苯环都能和氢气发生加成反应,所以1 mol A 可与4 mol H2发生反应,故D正确;
故选D.
点评 本题考查有机物结构和性质,明确官能团及其性质关系即可解答,侧重考查酚、醇、苯和烯烃性质,注意酚羟基和碳酸钠反应生成物,题目难度不大.


科目:高中化学 来源: 题型:解答题
| 元素 | I1 | I2 | I3 | I1+I2+I3 | I4 |
| Sc(钪) | 633 | 1235 | 2389 | 4257 | 7019 |
| Y(钇) | 616 | 1181 | 1980 | 3777 | 5963 |
| La(镧) | 538 | 1067 | 1850 | 3455 | 4819 |
| Ce(铈) | 527 | 1047 | 1949 | 3523 | 3547 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N层比M层少8个电子的元素 | B. | L层比M层多一个电子的元素 | ||
| C. | 最高价为+6价的元素 | D. | 无负化合价的元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通式相同的两种有机物按不同比例混合时,只要总质量一定,完全燃烧的耗氧量就一定 | |
| B. | 除去甲烷中的乙烯可用溴水或酸性高锰酸钾溶液 | |
| C. | 糖类、油脂、蛋白质都会在一定条件下水解 | |
| D. | 戊烷有3种同分异构体,而一氯戊烷有8种同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 氢化物 | A | B | C | D | E |
| 沸点/℃ | 1317 | 100 | 19.5 | -33 | -162 |

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 目前发现的所有元素占据了周期表里全部位置,不可能再有新的元素被发现 | |
| B. | 元素的性质随着原子序数的增加而呈周期性变化 | |
| C. | 俄国化学家道尔顿为元素周期表的建立作出了巨大贡献 | |
| D. | 可以利用元素周期律预测新元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

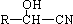 $\stackrel{H_{2}O/H+△}{→}$
$\stackrel{H_{2}O/H+△}{→}$ 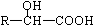
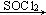
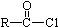 $\stackrel{R′OH}{→}$ RCOORˊ(R、Rˊ代表烃基)
$\stackrel{R′OH}{→}$ RCOORˊ(R、Rˊ代表烃基)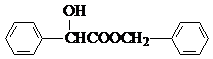 .
.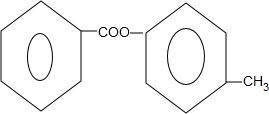 +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$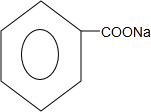 +
+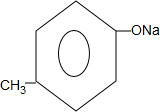 +H2O.
+H2O.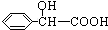 的同分异构体中:①能发生水解反应;②能发生银镜反应;③能与氯化铁溶液发生显色反应;④含氧官能团处在对位.满足上述条件的同分异构体共有3种(不考虑立体异构),写出核磁共振氢谱图中有五个吸收峰的同分异构体的结构简式
的同分异构体中:①能发生水解反应;②能发生银镜反应;③能与氯化铁溶液发生显色反应;④含氧官能团处在对位.满足上述条件的同分异构体共有3种(不考虑立体异构),写出核磁共振氢谱图中有五个吸收峰的同分异构体的结构简式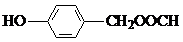 .
.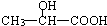 )的路线(其它试剂任选).
)的路线(其它试剂任选).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com