
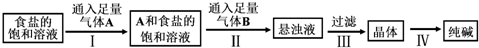
| A. | 气体A是NH3,气体B是CO2 | |
| B. | 侯氏制碱法的工艺过程中应用了物质溶解度的差异 | |
| C. | 第III步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒 | |
| D. | 第Ⅳ步操作的主要过程有溶解、蒸发、结晶 |
分析 向氨化的饱和食盐水中通入足量二氧化碳气体析出碳酸氢钠,利用CO2+NH3+HO2+NaCl═NaHCO3↓+NH4Cl的反应原理可制备碳酸氢钠,加热分解碳酸氢钠来制备碳酸钠,流程中A为氨气,B为二氧化碳,得到的悬浊液为NaHCO3,晶体为NaHCO3,以此解答该题.
解答 解:A.氨气易溶于水,二氧化碳能溶于水,依据侯德榜制碱的原理:向氨化的饱和食盐水中通入二氧化碳气体析出碳酸氢钠,加热反应制备纯碱,所以气体A为氨气,B为二氧化碳,故A正确;
B.侯氏制碱法利用的是碳酸氢钠溶解度比碳酸钠在同温下小的差异,在氨化饱和的氯化钠溶液里通足量CO2气体得到碳酸氢钠沉淀,故B正确;
C.第Ⅲ步操作是过滤操操作,通过过滤得到碳酸氢钠晶体,所以需要的仪器有:烧杯、漏斗、玻璃棒,故C正确;
D.第Ⅳ步操作是将晶体碳酸氢钠直接加热分解得到碳酸钠固体,故D错误;
故选D.
点评 本题考查了侯德榜制碱的工作原理和流程分析,题目难度中等,明确碳酸钠、碳酸氢钠、氨气、二氧化碳的性质,掌握工艺流程和反应原理是解题关键,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:解答题
 实验室需要0.1mol•L-1NaOH溶液500mL,根据溶液的配制情况,回答下列问题:
实验室需要0.1mol•L-1NaOH溶液500mL,根据溶液的配制情况,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 病人输液用的葡萄糖注射液是葡萄糖(化学式为C6H12O6)的水溶液,其标签上的部分内容如图所示.利用标签所提供的信息,回答下列问题:
病人输液用的葡萄糖注射液是葡萄糖(化学式为C6H12O6)的水溶液,其标签上的部分内容如图所示.利用标签所提供的信息,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2和3 | B. | 3和2 | C. | 3和1 | D. | 1和3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
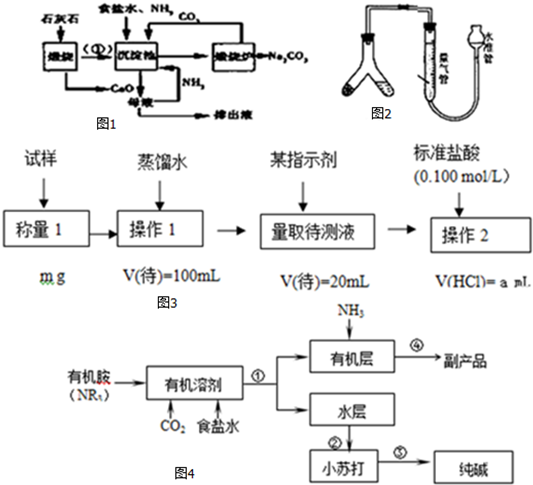
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向含有CaCO3沉淀的水中通入CO2至沉淀恰好溶解,再向溶液中加入NaOH饱和溶液,又有CaCO3沉淀生成 | |
| B. | 向Na2CO3溶液中逐滴加入等物质的量的稀盐酸,生成的CO2与原Na2CO3的物质的量之比为1:2 | |
| C. | 等质量的NaHCO3和Na2CO3分别与足量盐酸反应,在同温同压下,生成的CO2体积前者多 | |
| D. | 向Na2CO3饱和溶液中通CO2,有NaHCO3结晶析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
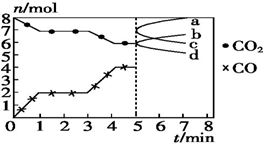 炼铁的还原剂CO是由焦炭和CO2反应而得.现将焦炭和CO2放入体积为2L的密闭容器中,高温下进行下列反应:C(s)+CO2(g)═2CO(g)△H=Q kJ•mol-1.如图为CO2、CO的物质的量n随时间t的变化关系图.下列说法正确的是( )
炼铁的还原剂CO是由焦炭和CO2反应而得.现将焦炭和CO2放入体积为2L的密闭容器中,高温下进行下列反应:C(s)+CO2(g)═2CO(g)△H=Q kJ•mol-1.如图为CO2、CO的物质的量n随时间t的变化关系图.下列说法正确的是( )| A. | 0~1 min,v(CO)=1 mol•L-1•min-1;1~3 min,v(CO)=v(CO2) | |
| B. | 当容器内的压强不变时,反应一定达到平衡状态,$\frac{P(平衡)}{P(起始)}$<1 | |
| C. | 3 min时,温度由T1升高到T2,则Q>0,再达平衡时,$\frac{K({T}_{2})}{K({T}_{1})}$>1 | |
| D. | 5 min时再充入一定量的CO,a、b曲线分别表示n(CO)、n(CO2)的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com