
【题目】在下列化学反应中,既有离子键、极性键、非极性键断裂,又有离子键、极性键、非极性键形成的( )
A.2Na2O2+2H2O=4NaOH+O2↑
B.Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑
C.Cl2+H2O=HClO+HCl
D.NH4Cl+NaOH ![]() NaCl+NH3↑+H2O
NaCl+NH3↑+H2O
【答案】A
【解析】解:A.该反应中2Na2O2+2H2O=4NaOH+O2↑中有离子键、极性键、非极性键断裂,又有离子键、极性键、非极性键形成,故A正确;
B.该反应Mg3N2+6H20=3Mg(OH)2↓+2NH3↑没有非极性键的断裂和形成,故B错误;
C.该反应Cl2+H2O=HClO+HCl中,没有离子键的断裂和形成,没有非极性共价键的形成,故C错误;
D.该反应NH4Cl+NaOH=NaCl+H20+NH3↑中没有非极性键的断裂和形成,故D错误;
故选A.
【考点精析】关于本题考查的极性键和非极性键,需要了解非极性键:由同种元素的原子间的原子间形成的共价键(共用电子对不偏移);极性键:由不同元素的原子间形成的共价键(共用电子对偏向吸引电子能力强的一方)才能得出正确答案.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某同学在实验报告中记录下列数据,其中正确的是
A. 用 25mL 量筒量取 12.36mL 盐酸
B. 用托盘天平称量 8.75g 食盐
C. 用 500mL 的容量瓶配制 450mL 溶液
D. 用 50mL 蒸馏烧瓶盛装 40mL 溶液进行蒸馏实验
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应能用 H+ + HCO3- = H2O + CO2↑的离子方程式表示的反应是( )
A. 碳酸氢钠溶液和稀硫酸的反应 B. 碳酸氢钠溶液和醋酸溶液的反应
C. 碳酸氢钾溶液和醋酸溶液的反应 D. 碳酸氢钡溶液与稀硫酸的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知固体Na2SO3受热易分解,实验流程和结果如下:
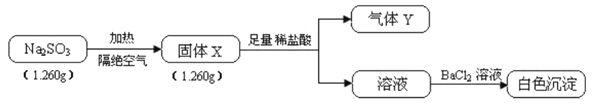
气体Y是一种纯净物,在标准状况下的密度为1.518g·L-1、请回答:
(1)气体Y分子的电子式___,白色沉淀的化学式_______。
(2)该流程中的Na2SO3受热分解的化学方程式__________。
(3)另取固体X试样和Na2SO3混合,加水溶解后与稀盐酸反应,有淡黄色沉淀产生,写出产生淡黄色沉淀的离子方程式____________(不考虑空气的影响)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验不能获得预期目的是( ) 
A.实验①烧杯中出现白色胶状沉淀,证明非金属性:N>C>Si
B.实验②烧杯中出现白色浑浊,说明镁与盐酸反应是放热反应
C.实验③a、b分别滴加2滴FeCl3溶液、CuSO4溶液,验证不同催化剂对反应速率的影响
D.实验④利用置换反应,证明金属单质还原性强弱,判断金属性强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列营养物质在人体内发生的变化及其对人的生命活动所起的作用叙述中,不正确的是( )
A. 淀粉![]() 葡萄糖
葡萄糖![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
B. 纤维素![]() 葡萄糖
葡萄糖![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
C. 油脂![]() 甘油和高级脂肪酸
甘油和高级脂肪酸![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
D. 蛋白质![]() 氨基酸
氨基酸![]() 人体所需的蛋白质(人体生长发育)
人体所需的蛋白质(人体生长发育)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图1)。从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化。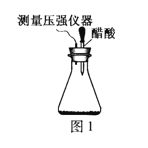
(1)请完成以下实验设计表(表中不要留空格):
编号 | 实验目的 | 碳粉/g | 铁粉/g | 醋酸/% |
① | 为以下实验作参照 | 0.5 | 2.0 | 90.0 |
② | 醋酸浓度的影响 | 0.5 | ______ | 36.0 |
③ | _________ | 0.2 | 2.0 | 90.0 |
(2)编号①实验测得容器中压强随时间变化如图2。t2时,容器中压强明显小于起始压强,其原因是铁发生了______腐蚀,负极的电极反应式为______。请在图3中用箭头标出发生该腐蚀时电子流动方向______;此时,碳粉表面发生了______(“氧化”或“还原”)反应。
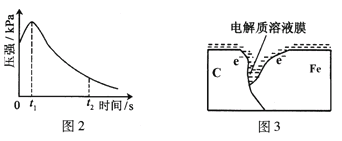
(3)该小组对图2中0~t1时压强变大的原因提出了如下假设,请你完成假设二:
假设一:发生析氢腐蚀产生了气体;
假设二:___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com