
【题目】已知X、Y、Z三种短周期元素的族序数之和为11,且X、Y、Z能形成化合物X2YZ3。下列判断正确的是
A. X、Y、Z不可能为同周期元素
B. 化合物X2YZ3可能难溶于水
C. Y的原子半径一定比Z小
D. X可能位于第IIA族
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列有关除杂方法正确的是
A. 除去Fe3+中Al3+:加入过量氨水充分反应后,过滤
B. 除去FeCl3中少量CuCl2:加入足量铁粉,过滤
C. 除去NaHCO3溶液中的Na2CO3:通入过量CO2充分反应
D. 除去铝粉中的镁粉:加入足量的氢氧化钠溶液后,过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃煤技术的改进,有助于合理控制温室效应、环境污染,并能进行资源化利用,还可重新获得燃料或重要工业产品。工业上以煤和水为原料通过一系列转化变为清洁能源氢气和工业原料甲醇。
(1)若碳的燃烧热为393.5kJ·mol-1,氢气的燃烧热为285.8kJ·mol-1。已知反应
C(s)+2H2O(g) ![]() CO2(g)+2H2(g) △H>0,能否求出该反应的△H_______(填“能”或“不能”)。若能则求出其△H(若不能请说明理由):_____________________。
CO2(g)+2H2(g) △H>0,能否求出该反应的△H_______(填“能”或“不能”)。若能则求出其△H(若不能请说明理由):_____________________。
(2)工业上也可以仅利用上述反应得到的CO2和H2进一步合成甲醇,反应方程式为:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H<0
CH3OH(g)+H2O(g) △H<0
①工业生产过程中CO2和H2的转化率________(填“前者大”、“后者大”、“一样大”或“无法判断”),为了提高甲醇的产率可以采取的措施是____________、____________(填两点)。
②在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2进行上述反应。测得CO2和CH3OH(g)浓度随时间变化如图所示。
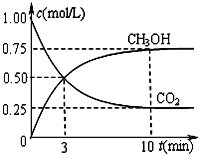
i.用H2表示0-3min内该反应的平均反应速率______________。
ii.该温度下的平衡常数为__________________。10 min后,保持温度不变,向该密闭容器中再充入1 mol CO2(g)和1 mol H2O(g),此时V正 _________V逆(填“>”、“<”或“=”)。
iii.对于基元反应aA+bB![]() cC+dD而言,其某一时刻的瞬时速率计算公式如下:正反应速率为V正=k正·c(A)a·c(B)b ;逆反应速率为V逆=k逆·c(C)c·c(D)d,其中k正、k逆为速率常数。若将上述反应视为基元反应则在上述条件下k逆∶k正=_________。反应进行到第3 min时V正 :V逆 =________。
cC+dD而言,其某一时刻的瞬时速率计算公式如下:正反应速率为V正=k正·c(A)a·c(B)b ;逆反应速率为V逆=k逆·c(C)c·c(D)d,其中k正、k逆为速率常数。若将上述反应视为基元反应则在上述条件下k逆∶k正=_________。反应进行到第3 min时V正 :V逆 =________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化合物的分子式为C5H11Cl,分析数据表明:分子中有两个—CH3、两个—CH2—、一个![]() 和一个—Cl,它的可能的结构有几种( )
和一个—Cl,它的可能的结构有几种( )
A. 3 B. 4 C. 5 D. 6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近《科学》杂志评出十大科技突破,其中“火星上‘找’到水的影子”排名笫一。下列关于水的说法中正确的是
A. 水的电离是放热的过程 B. 加入电解质一定会破坏水的电离平衡
C. 水的电离和电解都需要电 D. 水、乙酸和硫酸钡均属于电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有①甲烷、②乙烯、③苯、④聚乙烯、⑤丙炔、⑥环己烷、⑦邻二甲苯、⑧环己烯(![]() )。其中既能使KMnO4酸性溶液褪色又能与溴水反应使溴水褪色的是
)。其中既能使KMnO4酸性溶液褪色又能与溴水反应使溴水褪色的是
A.②④⑤⑧ B.②⑤⑧ C.②④⑤⑦ D.②④⑤⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一化学平衡状态体系中,发生下列量的变化,其中一定会使平衡发生移动的是( )
A. 反应物的转化率 B. 反应物的浓度
C. 正、逆反应速率 D. 体系的压强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com