
 、Ⅱ
、Ⅱ .
.

分析 (1)C6H6比饱和链烃(C6H14)少8个H,如果有叁键、环,结构中还可含有二个双键,根据叁键和双键可能的不同位置可确定可能的结构简式;
(2)①结构Ⅱ含有碳碳双键,根据碳碳双键的性质判断;根据根据及方程式计算需氢气的物质的量.
②根据换元法可知,该结构的四氯代物的种数和二氯代物的种数相同.根据等效氢,有1种氢原子,二氯代物的同分异构体可以采用固定一个氯原子的方法来寻找,即先进行一氯代物,产物有一种,再在一氯代物的基础用一个氯原子代替一个氢原子可得二氯代物,两个氯原子的位置只有三种情况:一是都位于正方形面的边上(连接两个三角形面的边),二是正方形面的对角线上,三是三角形面的边上;
(3)萘是一种芳香烃,含有苯环,不饱和度为$\frac{10×2+2-8}{2}$=7,含有两个苯环;
(4)萘分子碳碳之间的键是介于C-C单键与C=C双键之间的一种特殊的键.
解答 解:(1)C6H6比饱和链烃(C6H14)少8个H,如果有叁键、环,结构中还可含有二个双键,根据叁键和双键可能的不同位置可确定可能的结构简式为:
HC≡C-C≡C-CH2-CH3或HC≡C-CH2-C≡C-CH3或HC≡C-CH2-CH2-C≡CH或CH3-C≡C-C≡C-CH3,故答案为:HC≡C-C≡C-CH2-CH3或HC≡C-CH2-C≡C-CH3或HC≡C-CH2-CH2-C≡CH或CH3-C≡C-C≡C-CH3;
(2)①aⅠ碳碳之间的键是介于C-C单键与C=C双键之间的一种特殊键,不能被被酸性高锰酸钾溶液氧化,不能能与溴水发生加成反应,Ⅱ含有碳碳双键,能被被酸性高锰酸钾溶液氧化,能与溴水发生加成反应.结构都能与溴发生取代反应,都能与氢气发生加成反应.
Ⅰ结构为苯,1mol能与3mol氢气发生加成反应,Ⅱ结构中分子中含有2个C=C双键,所以1mol能与2mol氢气发生加成反应.
故答案为:ac;3;2;
②根据换元法可知,该结构的四氯代物的种数和二氯代物的种数相同.根据等效氢,该结构有1种氢原子,先进行一氯代物,产物有一种,再在一氯代物的基础用一个氯原子代替一个氢原子可得二氯代物,两个氯原子的位置只有三种情况:一是都位于正方形面的边上(连接两个三角形面的边),二是正方形面的对角线上,三是三角形面的边上,所以二氯代物有3种同分异构体.
故答案为:3;
(3)萘是一种芳香烃,含有苯环,不饱和度为$\frac{10×2+2-8}{2}$=7,含有两个苯环,结构简式为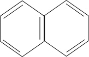 ,故答案为:C;
,故答案为:C;
(4)萘分子碳碳之间的键是介于C-C单键与C=C双键之间的一种特殊的键,故答案为:介于单键与双键之间的独特的键.
点评 本题考查苯的结构与性质,知识综合性较大,难度中等,要求学生具有整合知识的能力、对知识进行迁移运用.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
| 离子 | Fe 2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验目的或结论 |
| A | 向1mL0.2mol/LNaOH溶液中滴入2滴0.1mol/LMgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol/LFeCl3溶液,又生成红褐色沉淀 | 证明在相同温度下,溶解度:Mg(OH)2>Fe(OH)3 |
| B | 向两份等体积等浓度的H2O2溶液中,分别滴入等浓度等体积CuSO4、KMnO4溶液,后者产生气体较多 | 证明KMnO4溶液的催化效率更高 |
| C | 测定相同物质的量浓度的硅酸钠 和碳酸钠溶液的PH,前者较大 | 证明非金属性:C>Si |
| D | 向FeCl3溶液中加入铁钉,溶液颜色变浅 | 证明FeCl3溶液中存在水解平衡 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液质量与白色固体的质量均保持不变 | |
| B. | 溶液浓度和pH值均保持不变,溶液下部是1.73g氢氧化钡固体 | |
| C. | 溶液中钡离子与氢氧根离子的数目均保持不变,${\;}^{1{8}^{\;}}$O存在于溶液和固体中,固体质量大于1.73克 | |
| D. | 溶液中钡离子与氢氧根离子的物质的量的浓度保持不变,${\;}^{1{8}^{\;}}$O存在于溶液和固体中,固体质量大于1.73克 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2与O3 | B. | CH≡CH与CH2=CH2 | ||
| C. | ${\;}_{8}^{16}$O与${\;}_{8}^{18}$O | D. | CH3-CH2-CH2-CH3与CH3-CH2-CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
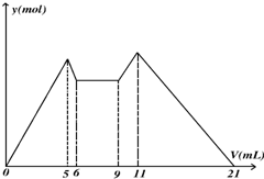
| A. | 原混合液中,c(Al3+):c(Mg2+):c(Cl-)=1:1:5 | |
| B. | A是NaOH,B是盐酸,且c(NaOH):c(HCl)=2:1 | |
| C. | 若A,B均为一元强酸或者一元强碱,则V(A):V(B)=7:13 | |
| D. | 从6到9,相应离子反应式H++OH-═H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+(aq)+OH-(aq)═H2O(l)△H=+57.3kJ•mol-1 | |
| B. | 加入少量蒸馏水,平衡①和②均向右移动 | |
| C. | 溶液中c(CH3COOH)>c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| D. | 加入少量CaCl2溶液,所得溶液中:c(CH3COOH)+2c(OH-)=c(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化铁 FeO 碱性氧化物 | B. | 碳酸气 CO 酸性氧化物 | ||
| C. | 硫酸 H2S 酸 | D. | 纯碱 Na2CO3 盐 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com