

分析 (1)由IO3-+5I-+6H+═3I2+3H2O可知,该反应需要酸性条件,需要碘离子,则选淀粉碘化钾试纸检验,以此解答;
(2)第1步:根据灼烧固体的装置回答,灼烧应在坩埚中进行;
第2步:海带灼烧成灰烬后,将灰烬转移到烧杯中,加适量的蒸馏水,用玻璃棒充分搅拌,煮沸后,过滤;
第3步:操作是通入氯气溶液,氯气氧化碘离子生成碘单质;
第4步:碘遇到淀粉变蓝色.
解答 解:(1)由IO3-+5I-+6H+═3I2+3H2O及I2遇淀粉变蓝可知,检验食盐中存在IO3-,该反应需要酸性条件,需要碘离子,则选淀粉碘化钾试纸检验,生成的I2由淀粉检验,
故答案为:②④;
(2)第1步:灼烧应在坩埚中进行,不能在试管、或烧杯中灼烧海带,
第2步:海带灼烧成灰烬后,将灰烬转移到烧杯中,加适量的蒸馏水,用玻璃棒充分搅拌,煮沸后,过滤,过程中需要的仪器为铁架台、烧杯、漏斗、玻璃管,
第3步:氧化.操作是通入氯气溶液,氯气氧化碘离子生成碘单质,
实际生产中常选择H2O2代替Cl2,避免引入氯离子,防止不会造成环境污染,
第4步:碘单质的检验.取少量第3步的溶液,滴加淀粉溶液,如果溶液显蓝色,则证明海带中含碘,
故答案为:坩埚;溶解;过滤;aefg;Cl2+2I-=I2+2Cl-;H2O2被还原为水,不会造成环境污染;淀粉.
点评 本题考查了海水提碘的过程分析判断、实验基本操作、物质检验等,掌握基础是解题关键,题目难度中等.


 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:高中化学 来源: 题型:选择题

| A. | 甲装置:可用来证明碳酸的酸性比硅酸强 | |
| B. | 乙装置:橡皮管的作用是能使水顺利流下 | |
| C. | 丙装置:用图示的方法不能检查此装置的气密性 | |
| D. | 丁装置:先从①口进气集满二氧化碳,再从②口进气,可收集氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2υ(正)(X)=3υ(逆)(Z) | B. | 混合气体的总质量不变 | ||
| C. | 混合气体的密度不变 | D. | △H的数值不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | b电极是负极 | |
| B. | 供电时的总反应为:2H2+O2═2H2O | |
| C. | 工作时溶液中阴离子移向正极 | |
| D. | 工作时正极区pH升高,负极区pH降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol羟基所含电子数为9NA | |
| B. | 常温、常压下,14g CO与N2的混合气含的原子数为NA | |
| C. | 标准状况下,22.4L CH3Cl所含原子数为5NA | |
| D. | 23gNa与足量H2O反应完全后可生成NA个H2分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该元素是非金属元素 | B. | 中子数为114 | ||
| C. | 其位置在第七周期IVA族 | D. | 质量数为114 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 124 g P4含有的P-P键的个数为6NA | |
| B. | 12 g石墨中含有的C-C键的个数为1.5NA | |
| C. | 12 g金刚石中含有的C-C键的个数为4NA | |
| D. | 60 g SiO2中含Si-O键的个数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
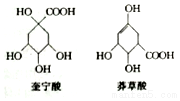 奎宁酸和莽草酸是某些高等植物特有的脂环状有机酸,常共存在一起,其结构简式如图所示.下列说法不正确的是( )
奎宁酸和莽草酸是某些高等植物特有的脂环状有机酸,常共存在一起,其结构简式如图所示.下列说法不正确的是( )| A. | 可用高锰酸钾溶液鉴别奎宁酸和莽草酸 | |
| B. | 奎宁酸的相对分子质量比莽草酸的大16 | |
| C. | 等物质的量的奎宁酸和莽草酸分别与足量Na反应,同温同压下产生H2的体积比为5:4 | |
| D. | 等物质的量的两种分别与足量NaOH溶液反应,消耗NaOH的物质的量相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com