
【题目】已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素。在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去)。

请回答下列问题:
(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,加热蒸干B的溶液不能得到B,则B的化学式可能是_____________;工业上制取A的离子方程式为________________。
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应则C的化学式是_____________ ①的化学方程式为______________________________。
(3)若D是氯碱工业的主要产品之一,B有两性,则反应②的离子方程式是________。
(4)若A、C、D都是常见气体,C是导致酸雨的主要气体,则反应③的化学方程式为________。某同学将搜集到的一定量的酸雨保存在密闭容器中,每隔一定时间测酸雨的pH,发现在起始一段时间内,酸雨的pH呈减小趋势,用离子方程式解释原因:_________________________________________。
【答案】 FeCl3 2Cl-+2H2O![]() 2OH-+Cl2↑+H2↑ NO2 4NH3+5O2
2OH-+Cl2↑+H2↑ NO2 4NH3+5O2![]() 4NO+6H2O Al(OH)3+OH-=AlO
4NO+6H2O Al(OH)3+OH-=AlO![]() +2H2O 2H2S+SO2=3S↓+2H2O 2H2SO3+O2=4H++2SO
+2H2O 2H2S+SO2=3S↓+2H2O 2H2SO3+O2=4H++2SO![]()
【解析】(1)氯气常用于自来水消毒,则A为Cl2;铁是使用最广泛的金属单质,D是铁,则B为FeCl3、C是FeCl2。
(2)碱性气体为NH3,汽车尾气中遇空气变色的气体是NO。
(3)常见的两性物质是Al2O3和Al(OH)3,D、C分别为NaOH和NaAlO2,故B为Al(OH)3。
(4)导致酸雨的主要气体是SO2,A与SO2均含有硫元素,且二者反应生成硫单质,故A为H2S。酸雨的主要成分是H2SO3,在放置过程中被氧化为H2SO4,酸性增强。


 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】向含SO![]() 、Fe2+、Br-、I-各0.1 mol的溶液中通入标准状况下的Cl2,通入Cl2的体积和溶液中相关离子的物质的量的关系图正确的是( )
、Fe2+、Br-、I-各0.1 mol的溶液中通入标准状况下的Cl2,通入Cl2的体积和溶液中相关离子的物质的量的关系图正确的是( )


A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下:

(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是__________________。
(2)第②步操作的目的是除去粗盐中的_________(填化学式),判断BaCl2已过量的方法是________________________________。
(3)在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是____________。
(4)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO4、Mg(OH)2、_____________。
(5)“蒸发结晶”用到的器材有:铁架台(铁圈)、坩埚钳、石棉网、火柴、玻璃棒、_____。
(6)第⑥步操作中涉及的化学方程式________________、________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用Na2FeO4溶液氧化废水中的还原性污染物M,为研究降解效果.设计如下对比实验探究温度、浓度、 pH、催化剂对降解速率和效果的影响,实验测得M的浓度与时间关系如图所示,
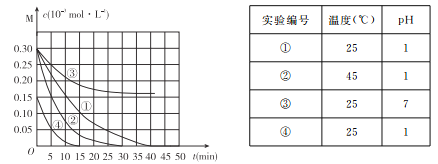
下列说法不正确的是
A. 实验①在15 min内M的降解速率为1.33×10-5mol/(L·min)
B. 若其他条件相同,实验①②说明升高温度,M降解速率增大
C. 若其他条件相同,实验①③证明pH越高,越不利于M的降解
D. 实验④说明M的浓度越小,降解的速率越快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定NaClO与NaClO3的物质的量之比为1∶3,则Cl2与NaOH溶液反应时被氧化的氯原子与被还原的氯原子的物质的量之比为( )
A. 4∶1 B. 1∶4 C. 3∶11 D. 11∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、钠、氯、铁等元素形成的单质及化合物在社会生活中应用广泛。请完成下列有关问题:
(1)工业用氯气与消石灰生产漂白粉,漂白粉的有效成分在水溶液中的电离方程式为______ 。
(2)氯化亚铁溶液中滴入几滴KSCN溶液无明显变化,再滴加少最氯水溶液变成红色,写出该变化过程中的化学方程式,开标出电子转移的方向与数目:______ 。
(3)实现C2O42-→CO2的转化必须加入______ (选填:氧化剂、还原剂、酸)。
(4)一个钠离子的质量为______ (保留三位有效数宁)。
(5)CO、CO2、O3(臭氧)三种气体,含有的氧原子数相等,则三种气体在同温同压下的体积比为______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】与外界隔热、容积不变的密闭容器中.发生2X(g) + Y(g)![]() 3Z(g) + M(s) △H=-akJ/mol,下列说法不正确的是
3Z(g) + M(s) △H=-akJ/mol,下列说法不正确的是
A. 容器的温度不再升高,表明反应达到平衡状态
B. 容器压强不变,表明反应达到平衡状态
C. 达到化学平衡时,反应放出的总热量可能为akJ
D. 反应过程中,气体的密度始终保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数约为6.02×1023/mol,下列说法一定正确的是( )
A. 60gSiO2晶体中,约含有2×6.02×1023个Si-O键
B. 78gNa2O2晶体中约有2×6.02×1023个阴离子
C. 720g C60晶体约含有6.02×1023个如图中晶胞单元

D. 14g两种烯烃CnH2n和CmH2m混合物,含有共用电子对数目约为3×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列氯化物中,既能由金属和氯气直接反应制得,又能由金属和盐酸反应制得的( )
A. CuCl2 B. FeCl2 C. AlCl3 D. FeCl3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com