
 ��
��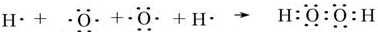 ��
��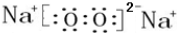 ���û������B��D�γɵ�ij�����ﷴӦ�Ļ�ѧ����ʽΪ��2Na2O2+2CO2=2Na2CO3+O2��lmolH�����÷�Ӧת�Ƶ�����Ϊ6.02��1023��NA��
���û������B��D�γɵ�ij�����ﷴӦ�Ļ�ѧ����ʽΪ��2Na2O2+2CO2=2Na2CO3+O2��lmolH�����÷�Ӧת�Ƶ�����Ϊ6.02��1023��NA������ A��B��C��D��E��F��G����Ԫ�أ�����A��B��C��D��E��FΪ������Ԫ����ԭ��������������A���������������۵Ĵ�����Ϊ�㣬��AΪHԪ��Ϊ��IVA��Ԫ�أ�������D2�����壬���ʱD2������ܶ�Լ��1.43g/L����Ħ������=1.43g/L��22.4L/mol=32g/mol��ΪOԪ�أ�
B�������������C���⻯����ˮ�з�Ӧ�õ���������X�ȿ����ᷴӦ�ֿ���Ӧ��B��Cԭ������С����Ԫ�أ���B������������Ƕ�����̼��C���⻯���ǰ��������߷�Ӧ����̼��炙�̼����泥�XΪ������X��̼��泥�����B��C��C��NԪ�أ���A��HԪ�أ�
Fԭ��M���ϵĵ��ӱ�K���5������Ϊ������Ԫ�أ���F��ClԪ�أ�Eԭ������С��F��
Eԭ�Ӱ뾶��ͬ�����г�ϡ�������������E��NaԪ�أ�
����G�ĺϽ������������������;��㣬��G��FeԪ�أ��ٽ����Ŀ�������
��� �⣺A��B��C��D��E��F��G����Ԫ�أ�����A��B��C��D��E��FΪ������Ԫ����ԭ��������������A���������������۵Ĵ�����Ϊ�㣬��AΪHԪ��Ϊ��IVA��Ԫ�أ�������D2�����壬���ʱD2������ܶ�Լ��1.43g/L����Ħ������=1.43g/L��22.4L/mol=32g/mol��ΪOԪ�أ�
B�������������C���⻯����ˮ�з�Ӧ�õ���������X�ȿ����ᷴӦ�ֿ���Ӧ��B��Cԭ������С����Ԫ�أ���B������������Ƕ�����̼��C���⻯���ǰ��������߷�Ӧ����̼��炙�̼����泥�XΪ���Σ���X��̼��泥�����B��C��C��NԪ�أ���A��HԪ�أ�
Fԭ��M���ϵĵ��ӱ�K���5������Ϊ������Ԫ�أ���F��ClԪ�أ�Eԭ������С��F��
Eԭ�Ӱ뾶��ͬ�����г�ϡ�������������E��NaԪ�أ�
����G�ĺϽ������������������;��㣬��G��FeԪ�أ�
��1��G��FeԪ�أ���Ԫ�����ڱ��е�λ���ǵ������ڵ�VIII�壬F����Ϊ�����ӣ������Ӻ�����3�����Ӳ㡢������������8����ClԪ�ص����ӽṹʾ��ͼ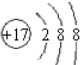 ��
��
�ʴ�Ϊ���������ڵ�VIII�壻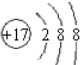 ��
��
��2��D��E��F�ֱ��������ӡ������Ӻ������ӣ����ӵ��Ӳ���Խ�������Ӱ뾶Խ���Ӳ�ṹ��ͬ�����ӣ����Ӱ뾶����ԭ�������������С����������3�����Ӳ㣬�������Ӻ���������2�����Ӳ㣬��D��E��F���Ӱ뾶�ɴ�С˳��Ϊ��Cl-��O2-��Na+��
�ʴ�Ϊ��Cl-��O2-��Na+��
��3��H��O���γ�ԭ�Ӹ�����Ϊ1��l�Ļ�����������⣬H��Oԭ��ͨ�����õ��Ӷ��γɹ������⣬�õ���ʽ��ʾ�û�������γɹ��̣�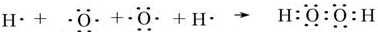 ��
��
�ʴ�Ϊ��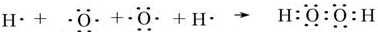 ��
��
��4��O��Na�γ�ij���ӻ�����H����Ư���ԣ�HΪ�������ƣ����������к������Ӽ����ۼ�����H�ĵ���ʽ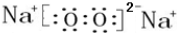 ���û������B��D�γɵ�ij�����������̼��Ӧ����̼���ƺ��������÷�Ӧ��ѧ����ʽΪ��2Na2O2+2CO2=2Na2CO3+O2���������ƺͶ�����̼�ķ�Ӧ����һ��Ĺ�������������������һ������ԭ����1mol�������Ʒ�Ӧת�Ƶ���1mol����lmolH�����÷�Ӧת�Ƶ�����Ϊ6.02��1023 �� NA��
���û������B��D�γɵ�ij�����������̼��Ӧ����̼���ƺ��������÷�Ӧ��ѧ����ʽΪ��2Na2O2+2CO2=2Na2CO3+O2���������ƺͶ�����̼�ķ�Ӧ����һ��Ĺ�������������������һ������ԭ����1mol�������Ʒ�Ӧת�Ƶ���1mol����lmolH�����÷�Ӧת�Ƶ�����Ϊ6.02��1023 �� NA��
�ʴ�Ϊ��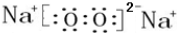 ��2Na2O2+2CO2=2Na2CO3+O2��6.02��1023 �� NA��
��2Na2O2+2CO2=2Na2CO3+O2��6.02��1023 �� NA��
��5����XΪ���Σ�Ϊ̼��泥�̼����к������Ӽ����ۼ����ʴ�Ϊ�����Ӽ����ۼ���
��6��N��Cl����Ԫ����Ƚϣ�ԭ�ӵõ���������ǿ��Ϊ�ȣ�
a��������Ԫ�صĵ��ʶ��Ƿ��Ӿ��壬���ʵ��۷е�����Ӽ��������йأ���õ������׳̶��أ����Բ��ܱȽϵõ�������ǿ�����ʴ���
b�������γɵĻ������У�FԪ�ص�ԭ���Ը��ۣ�˵��FԪ�صõ�����������B������ȷ��
c���Ƚ�������Ԫ�ص���̬�⻯����ȶ��ԣ�Ԫ�صķǽ�����Խǿ�����⻯����ȶ���Խǿ�����Կ�����õ�������ǿ��������ȷ��
�ʴ�Ϊ���ȣ�bc��
��7������Ԫ��Fe����Cl�γɻ�����FeCl3����Fe��ʯī�õ�����������FeCl3��Һ���γ�һ��ԭ��أ���ԭ��ع���ʱ��Fe��������ʯī��������������Feʧ���ӷ���������Ӧ�������������ӵõ��ӷ�����ԭ��Ӧ����ʯīһ�������ķ�Ӧ���Ա�ʾΪ2Fe3++2e-�T2Fe2+���������ӷ���ʽ2Fe3++Fe�T3Fe2+֪����Fe�ܽ�56gFeʱת��2mol���ӣ�����l.2mole-ת��ʱ����G�����仯=$\frac{1.2mol}{2mol}��56g/mol$=33.6g��
�ʴ�Ϊ��2Fe3++2e-�T2Fe2+��33.6��
��8������ȼ�ϼ��Ե���У�ͨ�������ĵ缫�Ǹ�����ͨ�������ĵ缫�����������Ϊ��������Ϊ������������ӦʽΪH2-2e-+2OH-=2 H2O��
�ʴ�Ϊ��H2-2e-+2OH-=2 H2O��
���� ���⿼��λ�ýṹ�������ϵ�����ã�Ϊ��Ƶ���㣬�漰ԭ���ԭ����������ԭ��Ӧ���㡢Ԫ�������ɡ���ѧ�����֪ʶ�㣬���ؿ���ѧ���ƶϡ�֪ʶ�ۺ�������������ȷ��ѧ��Ӧԭ����Ԫ�ػ��������ʡ�Ԫ���������ں��ǽⱾ��ؼ����ѵ��ǵ缫��Ӧʽ����д����Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ${\;}_{3}^{6}$Li��${\;}_{3}^{7}$Li | B�� | D2O��H2O | ||
| C�� | ${\;}_{6}^{14}$C��${\;}_{7}^{14}$N | D�� | ���ʯ��ʯī |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ���� | ���� |
| A | �����������ƴ���Һ�������ữ����������Һ����������±���� | �ԣ�±�����������������ƴ���Һ��������±���ƣ�±�����������ữ����������Һ��Ӧ������±�������� |
| B | ����������H218O��ˮ�⣬���������н�����18O | ������������ˮ����ɣ����������н�����18Oͬλ�أ����Ҵ��tû�� |
| C | ���������Ը��������Һ��ȥ�����е���ϩ���� | �ԣ���ϩ���������Ը��������Һ��Ӧ���������� CO2 |
| D | ���������Ƶ�Cu��OH��2����Һ�����Ҵ���Һ��������Һ����ȩ��Һ | �ԣ��Ҵ����������ȩ�����Ƶ�Cu��OH��2����Һ��Ӧ����Բ�ͬ������һ���Լ��� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2 �� | B�� | 3 �� | C�� | 4 �� | D�� | 5 �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 150 mL 1 mol•L-1�Ȼ�����Һ | B�� | 150 mL 3 mol•L-1�Ȼ�����Һ | ||
| C�� | 75 mL 2 mol•L-1�Ȼ����Һ | D�� | 50 mL 1 mol•L-1�Ȼ�ͭ��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
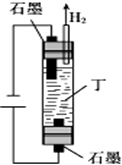 6�����ڶ���������Ԫ�ص����λ�����±���MԪ��ԭ�Ӻ����������YԪ��ԭ�Ӻ����������2����WԪ��ԭ�ӵĴ�����������������������2�����û�ѧ����ش��������⣺
6�����ڶ���������Ԫ�ص����λ�����±���MԪ��ԭ�Ӻ����������YԪ��ԭ�Ӻ����������2����WԪ��ԭ�ӵĴ�����������������������2�����û�ѧ����ش��������⣺| X | Y | Z | |
| W | M | Q |
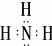 ��ʵ�����Ʊ��Ļ�ѧ����ʽ��2NH4Cl+Ca��OH��2$\frac{\underline{\;\;��\;\;}}{\;}$CaCl2+2NH3��+2H2O��������X������������Ӧ��ˮ������Һ��Ӧ�������ң�����Һ�е�����Ũ���ɴ�С��˳����c��NO3-����c��NH4+����c��H+����c��OH-����X�ĺ�18�����ӵ���̬�⻯��������������һ�ֻ����ͼ���ȼ�ϵ�أ���ع���ʱ�������ĵ缫��Ӧ����ʽ��N2H4-4e-+4OH-�TN2+4H2O��
��ʵ�����Ʊ��Ļ�ѧ����ʽ��2NH4Cl+Ca��OH��2$\frac{\underline{\;\;��\;\;}}{\;}$CaCl2+2NH3��+2H2O��������X������������Ӧ��ˮ������Һ��Ӧ�������ң�����Һ�е�����Ũ���ɴ�С��˳����c��NO3-����c��NH4+����c��H+����c��OH-����X�ĺ�18�����ӵ���̬�⻯��������������һ�ֻ����ͼ���ȼ�ϵ�أ���ع���ʱ�������ĵ缫��Ӧ����ʽ��N2H4-4e-+4OH-�TN2+4H2O���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ�Ӱ뾶��Cl��P | B�� | �⻯����ȶ��ԣ�CH4��SiH4 | ||
| C�� | ������ǿ����Na��Li | D�� | ���ԣ�H2CO3��H3PO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
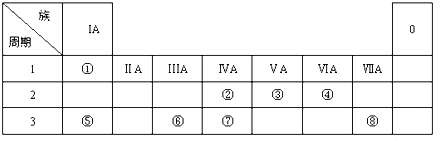
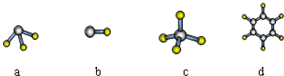
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com