
分析 (1)反应相当于Ba(OH)2先与H2SO4反应,然后再Na2SO4与氢氧化钡反应,100mLBa(OH)2溶液中n[Ba(OH)2]=0.1L×0.2moL•L-1=0.02mol,100mL溶液中n(H2SO4)=0.1L×0.1moL•L-1=0.01mol,故氢氧化钡与硫酸反应一半,硫酸钠反应一半,根据n=cV计算硫酸钠的物质的量,再根据m=nM计算硫酸钠的质量;
(2)溶液中沉淀量达到最大时,发生Ba2++SO42-=BaSO4↓,故n[Ba(OH)2]=n(SO42-),再根据V=$\frac{n}{V}$计算氢氧化钡的体积,溶液中溶质为NaOH.
解答 解:(1)反应相当于Ba(OH)2先与H2SO4反应,然后再Na2SO4与氢氧化钡反应,100mLBa(OH)2溶液中n[Ba(OH)2]=0.1L×0.2moL•L-1=0.02mol,100mL溶液中n(H2SO4)=0.1L×0.2moL•L-1=0.02mol,故氢氧化钡与硫酸恰好,硫酸钠不反应,反应的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2 H2O,溶液中溶质为Na2SO4,Na2SO4的物质的量为0.1L×0.1moL•L-1=0.01mol,Na2SO4的浓度=$\frac{0.01mol}{0.2L}$=0.05mol/L,
故答案为:Na2SO4;0.05;
(2)溶液中沉淀量达到最大时,硫酸根完全反应,发生Ba2++SO42-=BaSO4↓,故n[Ba(OH)2]=n(SO42-)=0.01mol+0.02mol=0.03mol,故氢氧化钡溶液的体积为$\frac{0.03mol}{0.2mol/L}$=0.15L=150mL.此时溶液中溶质为NaOH,故答案为:150;NaOH.
点评 本题考查混合物的有关计算、常用化学计量的有关计算等,难度中等,理解发生反应的本质和元素守恒是解题的关键.


科目:高中化学 来源: 题型:选择题
| A. | Na2SO4═Na++SO4-2 | B. | BaCl2═Ba2++Cl2- | ||
| C. | Al2(SO4)3═2Al3++3SO42- | D. | K2S═2K+S |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
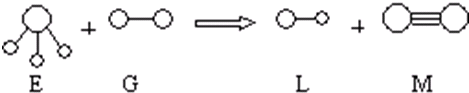
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
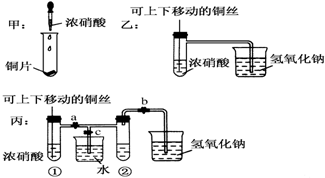
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯使溴的四氯化碳溶液褪色;苯使溴水褪色 | |
| B. | 由苯制环己烷;乙酸制乙酸乙酯 | |
| C. | 苯制溴苯;由乙烯制乙醇 | |
| D. | 乙烯使酸性高锰酸钾溶液褪色;乙醇与灼热的氧化铜反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
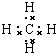 ,空间构型是正四面体,丙烷的结构简式为CH3CH2CH3,异丁烷的结构简式(CH3)2CH2CH3.
,空间构型是正四面体,丙烷的结构简式为CH3CH2CH3,异丁烷的结构简式(CH3)2CH2CH3.查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com