
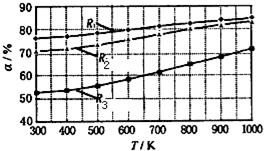
 ̼���������CH3OCOOC2H5����һ�������﮵���л����Һ������̼���������ԭ��Ϊ��C2H5OCOOC2H5��g ��+CH3OCOOCH3��g��?2CH3OCOOC2H5��g��������������ͬʱ��CH3OCOOCH3��ƽ��ת���ʣ��������¶ȣ�T������Ӧ����ȣ�R=n��C2H3OCOOC2H5����n��CH3OCOOCH3���Ĺ�ϵ��ͼ��ʾ�����ַ�Ӧ����ȷֱ�Ϊ1��1��2��1��3��1������˵������ȷ���ǣ�������
̼���������CH3OCOOC2H5����һ�������﮵���л����Һ������̼���������ԭ��Ϊ��C2H5OCOOC2H5��g ��+CH3OCOOCH3��g��?2CH3OCOOC2H5��g��������������ͬʱ��CH3OCOOCH3��ƽ��ת���ʣ��������¶ȣ�T������Ӧ����ȣ�R=n��C2H3OCOOC2H5����n��CH3OCOOCH3���Ĺ�ϵ��ͼ��ʾ�����ַ�Ӧ����ȷֱ�Ϊ1��1��2��1��3��1������˵������ȷ���ǣ�������| A�� | �÷�Ӧ���淴Ӧ��H��0 | |
| B�� | ����Ӧ����CH3OCOOCH3��Ũ�������̼���������ƽ��ת���� | |
| C�� | 650�棬��Ӧ�����Ϊ1��1ʱ��ƽ�ⳣ��K=6 | |
| D�� | ��C2H5OCOOC2H5��CH3OCOOC2H5�������ʱ�Ϊ1��2ʱ����Ӧ�ﵽƽ��״̬ |
���� A�����һ��ʱ������CH3OCOOCH3ת�������¶ȹ�ϵ���ж��¶ȶ�ƽ���ƶ���Ӱ�죻
B������һ�ַ�Ӧ���Ũ�ȣ��������������Ӧ���ת���ʣ�CH3OCOOCH3�ĺ���Խ�ߣ�C2H5OCOOC2H5��ת����Խ��
C����ͼ��֪��R3��ʾ��Ӧ�����Ϊ1��1��650��ʱCH3OCOOCH3��g����ת����Ϊ60%���Ӧ����ʼ���ʵ���Ϊ1mol��������ʽ����ƽ��ʱ����ֵ����ʵ������÷�Ӧǰ�������������䣬�������ʵ�������Ũ�ȴ���ƽ�ⳣ������ʽ���㣻
D����ͬ���ʱ�ʾ������������֮�ȵ��ڻ�ѧ������֮�ȣ����淴Ӧ����ƽ�⣮
��� �⣺A����ͼ��֪�����һ��ʱ���¶�Խ��CH3OCOOCH3��ƽ��ת����Խ�������¶�ƽ��������Ӧ�ƶ�����÷�Ӧ������ӦΪ���ȷ�Ӧ�����ԡ�H��0����A��ȷ��
B������һ�ַ�Ӧ���Ũ�ȣ��������������Ӧ���ת���ʣ�CH3OCOOCH3�ĺ���Խ�ߣ�C2H5OCOOC2H5��ת����Խ��B��ȷ��
C����ͼ��֪��R3��ʾ��Ӧ�����Ϊ1��1��650��ʱCH3OCOOCH3��g����ת����Ϊ60%���Ӧ����ʼ���ʵ���Ϊ1mol����
C2H5OCOOC2H5��g��+CH3OCOOCH3��g��?2CH3OCOOC2H5��g��
��ʼ��mol����1 1 0
�仯��mol����0.6 0.6 1.2
ƽ�⣨mol����0.4 0.4 1.2
�ʸ��¶���ƽ�ⳣ��k=$\frac{1��{2}^{2}}{0.4��0.4}$=9����C����
D��C2H5OCOOC2H5��CH3OCOOC2H5�������ʷֱ�Ϊ�淴Ӧ������Ӧ���ʣ�����֮��Ϊ1��2�����ڻ�ѧ������֮�ȱȣ���Ӧ�ﵽƽ�⣬��D��ȷ��
��ѡC��
���� ���⿼�����������ƽ���ƶ���Ӱ�죬��ȷ����ͼ���ǽⱾ��ؼ�����ѧƽ��״̬���жϼ�ƽ�ⳣ���ļ�����ѧϰ���ص㣬Ӧ���ص����գ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
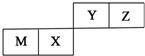 M��X��Y��Z�����ֳ����Ķ�����Ԫ�أ���Ԫ�������ڱ��е�λ����ͼ��ʾ������ֻ��M���ڽ���Ԫ�أ�����˵���У�������ǣ�������
M��X��Y��Z�����ֳ����Ķ�����Ԫ�أ���Ԫ�������ڱ��е�λ����ͼ��ʾ������ֻ��M���ڽ���Ԫ�أ�����˵���У�������ǣ�������| A�� | XԪ������������Ӧˮ�������������YԪ�ص� | |
| B�� | YԪ����̬�⻯����ȶ��Դ���ZԪ�ص� | |
| C�� | Ԫ��Z�����ڱ��е�λ��Ϊ��2���ڡ�VIA�� | |
| D�� | MԪ�ص�������ȿ�����ǿ����Һ��Ӧ��Ҳ������ǿ����Һ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��һ������ | ���Ӱ뾶 | �۵� | ���� |
| P��S | H-��Li+ | KCl��Si | HClO3��HClO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
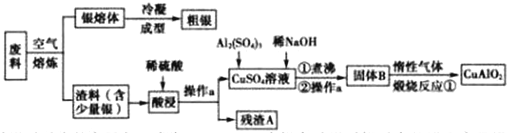
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ľ̿ | B�� | ��˿ | C�� | �ƾ� | D�� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������һ�������� | |
| B�� | 1�������������3��̼ԭ�Ӻ�3��ˮ���ӹ��� | |
| C�� | ��������������������ԭ��������ͬ | |
| D�� | �����Dz���Ϊ�����ṩ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
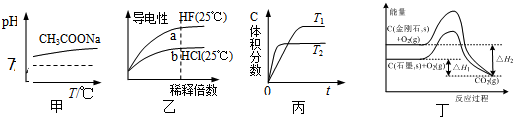
| A�� | ��ͼ��֪�������¶ȴ����Ƶ�ˮ��̶����� | |
| B�� | ��ͼ�ҿ�֪��a��Kw����ֵ��b��Kw����ֵ�� | |
| C�� | ��ͼ����֪����ӦA��g��+B��g��=2C��g�������ȷ�Ӧ | |
| D�� | ��ͼ����֪����ӦC�����ʯ��s��=C��ʯī��s�����ʱ��H=��H1-��H2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| R | T | |
| X | Y | Z |
| A�� | Rλ��Ԫ�����ڱ��еڶ����ڵ�VIA�� | |
| B�� | ����Ԫ����ԭ������������X | |
| C�� | ��̬�⻯���ȶ��ԣ�T��Y | |
| D�� | ZԪ�ص�����������Ӧ��ˮ����Ļ�ѧʽΪH2ZO4 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com