
(12分)(1)测定硫酸铜晶体结晶水的含量,若实验测得硫酸铜晶体中结晶水的含量偏低,造成此结果可能的原因有 (填序号)
①加热前所用的坩埚未完全干燥 ②加热时有少量的固体溅出 ③被测样品中含有加热易挥发的杂质 ④在空气中冷却后称量 ⑤加热至样品还有淡淡的蓝色时就称量
(2)已知H2、C2H4、C2H6各1mol分别充分燃烧生成液态水,放出热量分别为285.8kJ、1409.5kJ、1558kJ。试写出C2H4与H2生成C2H6的热化学方程式_______________ 。
(3)采用惰性电极从NO3-、SO42-、Cl-、Cu2+、Ba2+、Ag+、H+中选出适当的离子组成电解质,并电解:(填电解质的化学式)
①若两极分别放出H2和O2,电解质可能为______________________________。
②若阴极析出金属,阳极放出O2,电解质可能为__________________________。
③若两极均放出气体,且体积比为1 : 1,电解质可能为______________________。
④若既无O2也无H2放出,则电解质可能为_________________。
科目:高中化学 来源: 题型:
| W2-W3 |
| W2-Wl |
| W2-W3 |
| W2-Wl |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 剩余固体的质量 | 原始固体质量 |
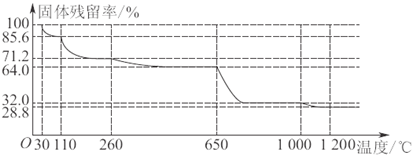
查看答案和解析>>
科目:高中化学 来源: 题型:
| 加热前的质量 | 加热后的质量 | |
| m0(坩埚) | m1(坩埚+晶体) | m2(坩埚+无水硫酸铜) |
| 18.269g | 19.420g | 19.011g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com