
分析 恒温下,将amol N2与bmol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g)??2ΝΗ3(g)
(1)依据化学平衡三段式列式计算
N2(g)+3H2(g)??2ΝΗ3(g)
起始量 a b 0
变化量 2 6 4
某时刻量 8 b-6 4
(2)N2(g)+3H2(g)??2ΝΗ3(g),反应后气体物质的量进行为生成氨气的物质的量,反应达平衡时,混合气体的体积为537.6L(标准状况下),其中NH3的体积分数为25%,平衡时混合气体物质的量:n平=$\frac{537.6L}{22.4L/mol}$=24mol
n平(NH3)=6mol
n始=30mol;
即a+b=30
因a=10,得到b为20,
(3)依据上述分析和计算得到平衡状态下各气体物质的量之比;
解答 解:(1)依据化学平衡三段式列式计算
N2(g)+3H2(g)??2ΝΗ3(g)
起始量 a b 0
变化量 2 6 4
平衡量 8 b-6 4
由反应的化学方程式得知,反应掉的N2和生成的NH3的物质的量之比为1:2,设反应掉的N2的物质的量为x.
则x:4mol=1:2
解得:x=2mol
若反应进行到某时刻t时,nt(N2)=8mol,nt(NH3)=4mol,
得到氮气的起始量:a=8mol+2mol=10mol;
答:若反应进行到某时刻t时,nt(N2)=8mol,nt(NH3)=4mol,得到a的值为10;
(2)平衡时混合气体物质的量:n平=$\frac{537.6L}{22.4L/mol}$=24mol
n平(NH3)=6mol
n始=30mol;
即a+b=30
因a=10,得到b为20,
所以a:b=10:20=1:2;
故答案为:1:2;
(3)N2(g)+3H2(g)??2ΝΗ3(g)
起始量 10 20 0
变化量 3 9 6
平衡量 7 11 6
平衡时:n(NH3)=6mol,n(N2)=7mol,n(H2)=11mol,
平衡混合气体中,n(N2):n(H2):n(NH3)=7:11:6;
故答案为:7:11:6.
点评 本题考查了化学平衡的分析应用,主要是反应特征和定量关系的分析应用,计算过程和方法是解题关键,掌握基础是解题关键,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
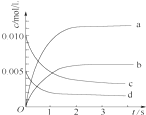 在2L密闭容器内,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间变化如表:
在2L密闭容器内,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间变化如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 温度K | 293 | 373 | 773 |
| 质量(g) | 133.6 | 106.6 | 91.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式相同的不同物质一定是同分异构体 | |
| B. | 通式相同的不同物质一定属于同系物 | |
| C. | 相对分子质量相同的不同物质一定是同分异构体 | |
| D. | 分子式相同,元素的质量分数也相同的物质是同种物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
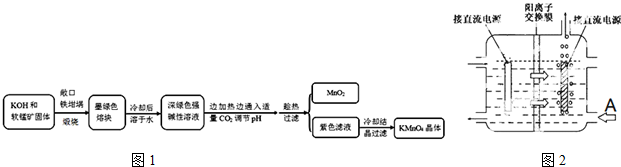
| 物质 | KMnO4 | K2CO3 | KHCO3 | K2SO4 | CH3COOK |
| 20℃溶解度 | 6.4 | 111 | 33.7 | 11.1 | 217 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸具有吸水性,可用于干燥二氧化碳、硫化氢等气体 | |
| B. | 氨气极易溶于水,可用作制冷剂 | |
| C. | 浓硝酸在常温下能使铝钝化,可用铝槽车运输浓硝酸 | |
| D. | SO2具有强还原性,在空气中极易被氧化为SO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com