
| A.溶于水 | B.通入CCl4 |
| C.通入NaOH溶液 | D.用湿润的淀粉KI试纸 |
 HBr+HBrO,Br2水中仍有大量Br2分子存在,溶液是橙色,与前者可区别开。
HBr+HBrO,Br2水中仍有大量Br2分子存在,溶液是橙色,与前者可区别开。 N2O4+Q这个平衡的热效应,将两盛气体的玻璃容器同时置于热水或冷水中,观察气体颜色变化,有变化的是NO2气体。
N2O4+Q这个平衡的热效应,将两盛气体的玻璃容器同时置于热水或冷水中,观察气体颜色变化,有变化的是NO2气体。

科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.硝酸与金属反应时,不会表现出酸性 |
| B.浓硝酸与浓盐酸按1∶3的体积比所得的混合物叫王水 |
| C.硝酸电离出的H+离子,能被锌、铁等金属还原成H2 |
| D.常温下,向浓硝酸中投入铁片,会产生大量的红棕色气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
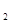 的化学方程式:______________;___________________。
的化学方程式:______________;___________________。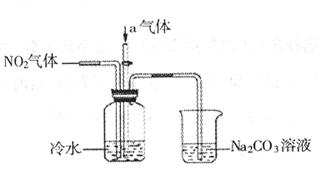
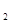 CO
CO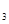 溶液的烧杯为尾气处理装置,该装置中反应的化学方程式是:
溶液的烧杯为尾气处理装置,该装置中反应的化学方程式是: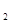 +_______Na
+_______Na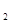 CO
CO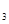 +_______H
+_______H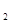 O=NaNO
O=NaNO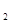 +_______+_______NaHCO
+_______+_______NaHCO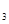 (完成此方程式)
(完成此方程式)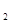 O
O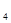 代替NO
代替NO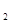 与水和a气体反应可生成硝酸,此反应的化学方程式是:
与水和a气体反应可生成硝酸,此反应的化学方程式是:查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
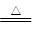 2KNO2+O2↑,
2KNO2+O2↑,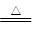 2CuO+4NO2↑+O2↑, 4AgNO3
2CuO+4NO2↑+O2↑, 4AgNO3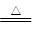 4Ag+4NO2↑+2O2↑
4Ag+4NO2↑+2O2↑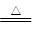 M(NO2)2+O2↑
M(NO2)2+O2↑  2MO+4NO2↑+O2↑
2MO+4NO2↑+O2↑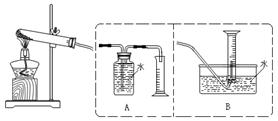
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.上述反应,每生成lmolN2O,消耗67.2LCO |
| B.等物质的量的N2O和CO2含有相等的电子数 |
| C.N2O只有氧化性,无还原性 |
| D.N2O会迅速与人体血红蛋白结合,使人中毒 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加水,将湿润的红色石蕊试纸放在试管口 |
| B.加NaOH溶液,加热,滴入紫色石蕊试剂 |
| C.加NaOH溶液,加热,滴入酚酞试剂 |
| D.加NaOH溶液,加热,将湿润的红色石蕊试纸放在试管口 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com