
| A. | 氢氧化钠与稀盐酸反应 | B. | 锌与稀硫酸反应 | ||
| C. | Ba(OH)2•8H2O与NH4Cl反应 | D. | 灼热的炭与二氧化碳反应 |
 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 一般碳碳σ键比π键重叠程度大,形成的共价键强 | |
| B. | 分子中含有共价键,则至少含有一个σ键 | |
| C. | 在气体单质中,一定有σ键,可能有π键 | |
| D. | CH4分子中的碳原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成4个C-H σ键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤的液化过程为物理过程 | |
| B. | 甲烷和乙烯都可以与氯气反应 | |
| C. | 酸性高锰酸钾可以氧化苯和甲烷 | |
| D. | 乙烯可以与氢气发生加成反应,苯不能与氢气加成 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
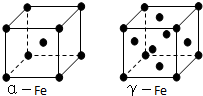
| A. | 空间利用率α-Fe大于γ-Fe | |
| B. | α-Fe、γ-Fe晶胞中铁原子个数比为1:2 | |
| C. | 金属铁的导电性是由于通电时自由电子作定向移动 | |
| D. | α-Fe延展时,可以转变为γ-Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
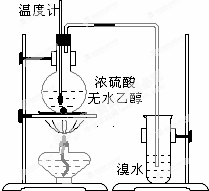 为探究实验室制乙烯及乙烯和溴水的加成反应.甲同学设计了如图所示的实验装置,并进行了实验.当温度升至170℃左右时,有大量气体产生,产生的气体通入溴水中,溴水的颜色迅速褪去.甲同学认为达到了实验目的.
为探究实验室制乙烯及乙烯和溴水的加成反应.甲同学设计了如图所示的实验装置,并进行了实验.当温度升至170℃左右时,有大量气体产生,产生的气体通入溴水中,溴水的颜色迅速褪去.甲同学认为达到了实验目的.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 半径:F->Na+>Mg2+>Al3+ | B. | 沸点:H2O<H2S<H2Se | ||
| C. | 酸性:HClO4>H2SO4>H3PO4 | D. | 熔点:SiO2>NaCl>CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ①③ | C. | ①②③ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
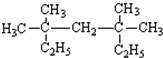 系统命名为:3,3,5,5-四甲基庚烷.
系统命名为:3,3,5,5-四甲基庚烷.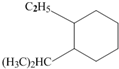 的炔烃的结构简式:
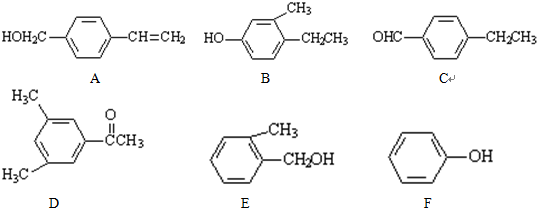
的炔烃的结构简式: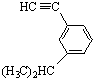 .
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com