
| A. | 常温常压下,32g氧气所含的原子数为NA | |
| B. | 标准状况下,22.4L 四氯化碳的分子数为NA | |
| C. | 0℃,101KPa下,44.8L氮气所含有的分子数为2NA | |
| D. | 常温常压下,1mol氦气含有的分子数为2NA |
分析 A、氧气由氧原子构成;
B、标况下,四氯化碳为液态;
C、标况下,气体摩尔体积为22.4L/mol;
D、根据分子个数N=nNA来计算.
解答 解:A、氧气由氧原子构成,故32g氧气中含有的氧原子的物质的量n=$\frac{32g}{16g/mol}$=2mol,即2NA个,故A错误;
B、标况下,四氯化碳为液态,不能根据气体摩尔体积来计算其物质的量和分子个数,故B错误;
C、0℃,101KPa下俗称标况,而标况下,气体摩尔体积为22.4L/mol,故44.8L氮气的物质的量n=$\frac{44.8L}{22.4L/mol}$=2mol,故含有的氮气分子为2NA个,故C正确;
D、1mol氦气中含有的分子个数N=nNA=NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:选择题
| A. | Cl- 不可能存在 | B. | 100 mL溶液中含0.01 mol CO32- | ||
| C. | K+一定存在 | D. | Ba2+一定不存在,Mg2+可能存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
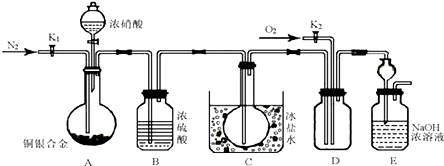
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 要想使AlCl3溶液中的Al3+几乎全部沉淀出来,可以加入过量的氨水 | |
| B. | 向FeCl2溶液中加入氨水,最终会看到红褐色沉淀 | |
| C. | 漂白粉的有效成分是次氯酸钙 | |
| D. | 氢氧化钠、纯碱溶液要存放在带磨砂玻璃塞的试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L | B. | 0.5mol/L | C. | 4mol/L | D. | 1mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
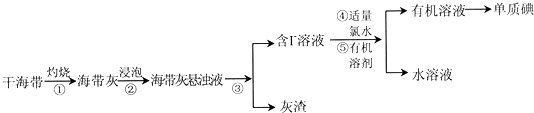
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2KNO3═2KNO2+O2↑ | B. | NH4HCO3═NH3↑+CO2↑+H2O | ||
| C. | 3NO2+H2O═2HNO3+NO | D. | SO2+2H2S═3S↓+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com