
 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案科目:高中化学 来源:2015-2016学年河北省高二下期末化学试卷(解析版) 题型:选择题
下列物质的使用不涉及化学变化的是( )
A.明矾用作净水剂 B.液氨用作致冷剂
C.氢氟酸刻蚀玻璃 D.生石灰作干燥剂
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古高二实验班下期中化学卷(解析版) 题型:选择题
用价层电子对互斥理论预测H2S和BF3的立体结构,两个结论都正确的是( )
A.直线形;三角锥形
B.V形;三角锥形
C.直线形;平面三角形
D.V形;平面三角形
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二下期末化学试卷(解析版) 题型:填空题
氮元素可形成卤化物、叠氮化物及配合物等
(1)在铜催化作用下F2和过量NH3反应得到NF3,其构型为三角锥形,沸点-129℃,则NF3属于____________晶体。
(2)氢叠氮酸(HN3)是一种弱酸,它的酸性类似于醋酸,微弱电离出H+和N3-.
①与N3-互为等电子体的分子有:____________(举1例),由此可推知N3-的空间构型是____________型;
②叠氮化物、氰化物能与Fe3+及Cu2+及Co3+等形成络合物,如:[Co(N3)(NH3)5]SO4、Fe(CN)64-。写出钴原子在基态时的价电子排布式:____________ ;[Co(N3)(NH3)5]SO4中钴的配位数为____________;CN-中C原子的杂化类型是____________;
(3)由叠氮化钠(NaN3)热分解可得纯N2:2NaN3(s)=2Na(l)+3N2(g),有关说法正确的是____________(选填序号)
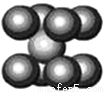
A.NaN3与KN3结构类似,前者晶格能较小
B.第一电离能(I1):N>P>S
C.钠晶胞结构如图,该晶胞分摊2个钠原子
D.氮气常温下很稳定,是因为氮的电负性大
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二下期末化学试卷(解析版) 题型:选择题
下列图示与对应的叙述相符的是( )
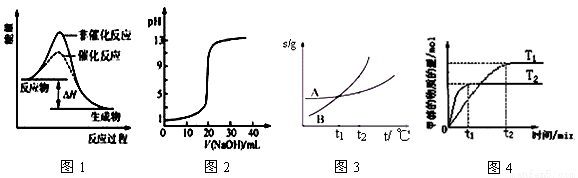
A.图1表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化
B.图2表示0.1000 mol•L-1NaOH溶液滴定20.00mL0.1000 mol•L-1CH3COOH溶液所得到的滴定曲线
C.图3表示A、B两物质的溶解度随温度变化情况,将tl℃时A、B的饱和溶液分别升温至t2℃时,溶质的质量分数B=A
D.图4表示在其他条件相同时,分别在T1、T2温度下由CO2和H2合成甲醇的物质的量随时间变化情况,则CO2和H2合成甲醇是吸热反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二下期末化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中能大量共存的是( )
A.滴入酚酞显红色的溶液:Na+、Al3+、SO42-、Cl-
B.滴入KSCN显红色的溶液:Na+、Cu2+、Br-、SO42-
C.c(Fe2+)=1mol/L的溶液:H+、Na+、Cl-、NO-3
D.加入铝粉能产生大量H2的溶液:Na+、K+、Cl-、HCO3-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年西藏日喀则一中高二月考化学试卷(解析版) 题型:填空题
本题为《化学反应原理(选修4)》选做题。
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理。请回答下列问题:
(1)常温下,某纯碱(Na2CO3)溶液中滴入酚酞,溶液呈红色,则该溶液呈_____性,原因是___________;(用离子方程式表示)
(2)在常温下将pH=2的盐酸10mL加水稀释到1L,则稀释后的溶液的pH值等于___________;
(3)已知在H2S溶液中存在下列平衡:H2S HS-+H+
HS-+H+
①向H2S溶液中加入NaOH固体时,(不考虑温度变化)电离平衡向______移动,(填“左”或“右”)c(H+)_________。(填“增大”、“减小”或“不变”)
②向H2S溶液中加入NaHS固体时,电离平衡向______移动,(填“左”或“右”)c(S2-)_________。(填“增大”、“减小”或“不变”)
(4)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图1所示.则图中表示醋酸溶液中pH变化曲线的是________(填“A”或“B”);
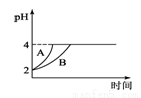
(5)难溶电解质在水溶液中存在溶解平衡。某MgSO4溶液里c(Mg2+)=0.002mol•L-1,如果生成Mg(OH)2沉淀,应调整溶液pH,使之大于________;(该温度下Mg(OH)2的Ksp=2×10-11)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年西藏日喀则一中高二月考化学试卷(解析版) 题型:选择题
CH4与Cl2在光照条件下反应生成多种产物,其中物质的量最大的是
A.HCl B.CCl4 C.CH3Cl D.H2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二下期末化学试卷(解析版) 题型:选择题
下列根据有关“规律”推出的结论合理的是
A. 根据同周期元素的第一电离能变化趋势,推出Al的第一电离能比Mg大
B. 根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7
C. 根据溶液的pH与溶液酸碱性的关系,推出pH=6.8的溶液一定显酸性
D. 根据较强酸可以制取较弱酸的规律,推出CO2通入NaClO溶液中能生成HClO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com