
研究人员研制利用低品位软锰矿浆(主要成分是MnO2)吸收硫酸厂的尾气SO2,制备硫酸锰的生产流程如下:
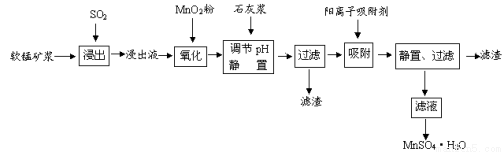
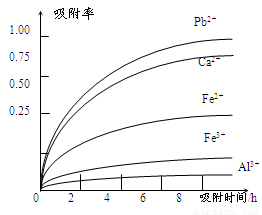
已知:浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+、Ca2+、Pb2+等其他金属离子。PbO2的氧化性大于MnO2。PbSO4是一种微溶物质。有关金属离子的半径、形成氢氧化物沉淀时的pH见下表,阳离子吸附剂吸附金属离子的效果见下图。
离子 | 离子半径(pm) | 开始沉淀 时的pH | 完全沉淀 时的pH |
Fe2+ | 74 | 7.6 | 9.7 |
Fe3+ | 64 | 2.7 | 3.7 |
Al3+ | 50 | 3.8 | 4.7 |
Mn2+ | 80 | 8.3 | 9.8 |
Pb2+ | 121 | 8.0 | 8.8 |
Ca2+ | 99 | - | - |
请回答下列问题:
(1)写出浸出过程中生成Mn2+反应的化学方程式 。
(2)氧化过程中主要反应的离子方程式 。
(3)在氧化后的液体中加入石灰浆,用于调节pH值,此处调节pH值用到的仪器是 ,应调节pH的范围为 。
(4)阳离子吸附剂可用于除去杂质金属离子。请依据图、表信息回答,决定阳离子吸附剂吸附效果的因素有 、 等;吸附步骤除去的主要离子为: 。
(5)CaSO4是一种微溶物质,已知Ksp(CaSO4)=9.10×10—6。现将c mol·L—1CaCl2溶液与2.00×10—2 mol·L—1Na2SO4溶液等体积混合(忽略体积的变化),则生成沉淀时,c的最小值是 。
(1)SO2+MnO2=MnSO4 (2)2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O;
(3)pH计, 4.7 ≤pH<8.3 (4)吸附时间、金属离子的半径 、金属离子的电荷;Pb2+、Ca2+
(5)1.82×10 - 3
【解析】
试题分析:(1)根据题意在浸出过程中生成Mn2+反应的化学方程式为SO2+MnO2=MnSO4;(2)将Fe2+氧化为Fe3+过程中主要反应的离子方程式为2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O。(3)在氧化后的液体中加入石灰浆,用于调节pH值,此处调节pH值用到的仪器是pH计。使Fe3+沉淀完全的pH为3.7,而Mn2+开始形成沉淀的pH为8.3。因此应调节pH的范围为4.7 ≤pH<8.3。(4)根据题目提供的表格数据可知决定阳离子吸附剂吸附效果的因素有吸附时间、金属离子的半径 、金属离子的电荷;吸附步骤除去的主要离子为Pb2+、Ca2+。(5)CaSO4是一种微溶物质,已知Ksp(CaSO4)=9.10×10—6。现将c mol/LCaCl2溶液与2.00×10—2 mol/LNa2SO4溶液等体积混合,由于忽略体积的变化,所以混合后氯化钙和硫酸钠溶液的浓度都要减半;c(SO42-)=1.00×10—2 mol/L. c(Ca2+)=c/2mol/L.由于Ksp(CaSO4)= 9.10×10—6,c(SO42-)·c(Ca2+)≥9.10×10—6,则生成沉淀时c(Ca2+)≥(9.10×10—6÷1.00×10—2 mol/L)×2=1.82×10-3mol/L。因此c的最小值是1.82×10-3mol/L.
考点:考查化学反应原理、影响离子吸收的因素及沉淀溶解平衡和溶度积的计算的知识。


科目:高中化学 来源:2013-2014学年广东省茂名市高三第二次高考模拟理综化学试卷(解析版) 题型:填空题
Suzuki偶联反应在有机合成上有广泛应用,该方法可以应用于合成昆虫信息素。其反应①如下(Ph-代表苯基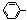 ):
):
反应①: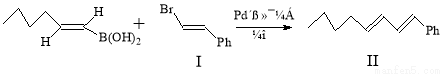
化合物I可以由以下途径合成:
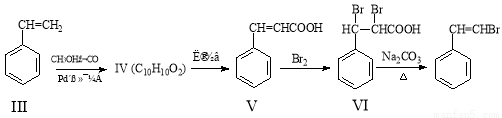
(1)化合物I的分子式为 ,1mol化合物III完全燃烧消耗氧气 mol。
(2)化合物IV的结构简式为 ,化合物V转化为化合物VI的反应类型为 。
(3)写出化合物VI在足量的NaOH溶液中共热反应的方程式 。
(4)已知化合物Ⅶ是化合物V的同分异构体,化合物Ⅶ的核磁共振氢谱中有 4种峰,峰面积之比为3:2:2:1,且1mol Ⅶ与足量银氨溶液反应生成4mol Ag单质,写出化合物Ⅶ的结构简式 。
(5)化合物( )与化合物(
)与化合物(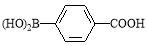 )能发生偶联反应生成一种抗抑郁药物,写出该抗抑郁药物的结构简式 。
)能发生偶联反应生成一种抗抑郁药物,写出该抗抑郁药物的结构简式 。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省清远市高三4月模拟理综化学试卷(解析版) 题型:选择题
如下实验操作正确且能达到实验目的的是
A.将十水碳酸钠置于蒸发皿中,加热脱去结晶水
B.用分液漏斗分离溴乙烷与氢氧化钠溶液发生反应后的生成物
C.用铁粉与稀硝酸反应,制取少量氢气,用排水法收集
D.用酸式滴定管量取6.55 mL的KMnO4溶液
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省惠州市高三4月模拟考试理综化学试卷(解析版) 题型:填空题
铬铁矿的主要成分的化学式为FeO·Cr2O3,还含有SiO2、Al2O3等杂质。工业上常采用固体碱熔氧化法用铬铁矿粉制备重铬酸钾,流程为:

已知:①NaFeO2遇水强烈水解;
②重铬酸钾为橙红色针状晶体,溶于水,不溶于乙醇,有强氧化性;
③2CrO42- + 2H+  Cr2O72-+ H2O
Cr2O72-+ H2O
(1)灼烧操作一般在坩埚中进行,下列物质适合用来制作此实验坩埚材料的是
A.铁 B.氧化铝 C.石英 D.陶瓷
(2)①铬铁矿经粉碎处理的目的是 。
②写出Cr2O3和纯碱、氧气反应生成Na2CrO4的化学方程式为 ;
③NaFeO2水浸时强烈水解生成氢氧化铁沉淀,离子方程式为___ ___。
(3)滤液1的成分除Na2CrO4、NaOH外,还含有(填化学式) ,
(4)通过途径Ⅰ从Na2CrO4溶液获得K2Cr2O7晶体,操作步骤有:“酸化”→加KCl固体→蒸发浓缩→操作a→过滤→洗涤→干燥。
① “酸化”步骤用醋酸调节溶液pH<5,其目的是 ;
②操作a的名称 。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省惠州市高三4月模拟考试理综化学试卷(解析版) 题型:选择题
下列各组离子,在碱性条件下能大量共存,在强酸性条件下发生氧化还原反应的是
A.Mg2+、Na+、SO42-、HCO3— B.Na+、K+、NO3—、SO32—
C.K+、Na+、SiO32—、ClO— D.NH4+、Na+、SO42—、NO3—
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省广州市番禺区高考统考(一)理综化学试卷(解析版) 题型:选择题
下列有关物质的性质与其应用不相对应的是( )
A.Al具有良好延展性和抗腐蚀性,可制成铝箔包装物品
B.NaHCO3能与碱反应,食品工业用作焙制糕点的膨松剂
C.NH3能与Cl2生成NH4Cl,可用浓氨水检验输送氯气的管道是否有泄漏
D.K2FeO4能与水作用生成Fe(OH) 3胶体和O2,可用于自来水的净化和杀菌消毒
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省广州市毕业班综合测试(二)理综化学试卷(解析版) 题型:填空题
碲(Te)为ⅥA族元素,是当今高新技术新材料的主要成分之一。工业上可从电解精炼铜的阳极泥中提取碲。
(1)粗铜中含有Cu和少量Zn、Ag、Au、TeO2及其他化合物,电解精炼后,阳极泥中主要含有TeO2、少量金属单质及其他化合物。电解精炼粗铜时,阳极电极反应式为 。
(2)TeO2是两性氧化物,微溶于水,可溶于强酸或强碱。从上述阳极泥中提取碲的一种工艺流程如下:
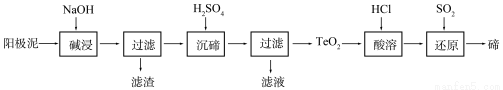
①“碱浸”时TeO2发生反应的化学方程式为 。
②“沉碲”时控制溶液的pH为4.5-5.0,生成TeO2沉淀。如果H2SO4过量,溶液酸度过大,将导致碲的沉淀不完全,原因是 ;防止局部酸度过大的操作方法是 。
③“酸溶”后,将SO2通入TeCl4溶液中进行“还原”得到碲,该反应的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省十校联考高三下学期理综化学试卷(解析版) 题型:选择题
下列陈述I、II正确并且有因果关系的是
选项 | 陈述I | 陈述II |
A | Fe3+有氧化性 | 实验室常用KSCN溶液检验Fe3+ |
B | SO2有较强的还原性 | SO2可使酸性KMnO4溶液褪色 |
C | Mg有还原性 | 电解MgCl2饱和溶液可制备Mg |
D | 浓H2SO4有吸水性 | 浓H2SO4可用于干燥氨气 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年天津市高三年级4月考理综化学试卷(解析版) 题型:填空题
已知有机物A分子由C、H、O三种元素组成,其蒸汽密度是相同条件下氢气密度的60倍,0.1molA在足量的氧气中充分燃烧后生成0.8molCO和7.2gH2O,A可以发生银镜反应,其苯环上的一氯代物有3种。
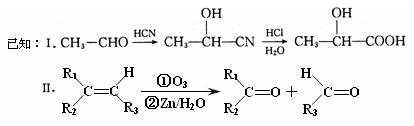
现有如下转化关系: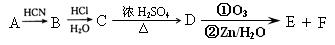 其中D能使溴的四氯化碳溶液褪色,F将继续氧化生成G,G的相对分子质量为90。
其中D能使溴的四氯化碳溶液褪色,F将继续氧化生成G,G的相对分子质量为90。
(1)A中含氧官能团的名称是 ,A的结构简式为 。
(2)C可能具有的化学性质有 (填序号)。
①能与H2发生加成反应
②能在碱性溶液中发生水解反应
③能与甲酸发生酯化反应
④能与Ag(NH3) 2OH溶液发生银镜反应
⑤能与NaOH溶液反应
A.①②③ B.①③⑤ C.①②③⑤ D.②③④⑤
(3) ① 写出C→D的化学反应方程式_______ ;反应类型为_____________________。
② 催化剂条件下,D生成高聚物的化学方程式 ;
③ G与足量NaHCO3溶液反应的化学方程式 。
(4)C的同分异构体有多种,其中符合下列要求的有机物有两种:
①属于酯类化合物 ②遇三氯化铁溶液显紫色
③与新制氢氧化铜悬浊液共热可生成红色沉淀 ④苯环上的一卤代物只有一种
写出其中一种有机物的结构简式 。
(5)聚乳酸( )可以生物降解,请写出以2-丁烯为原料制备聚乳酸的合成路线流程图(无机试剂任选)。
)可以生物降解,请写出以2-丁烯为原料制备聚乳酸的合成路线流程图(无机试剂任选)。
合成路线示例: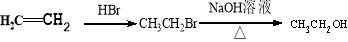
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com