
 FeO(s)+H2(g) △H1 平衡常数为K1
FeO(s)+H2(g) △H1 平衡常数为K1  H2(g)+CO2(g) △H2 平衡常数为K2
H2(g)+CO2(g) △H2 平衡常数为K2  FeO(s)+CO(g) △H3 平衡常数为K3
FeO(s)+CO(g) △H3 平衡常数为K3


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
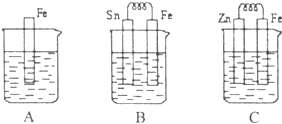 I.A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸.
I.A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸.查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用浓盐酸、MnO2共热制Cl2,再用Cl2和Ca(OH)2反应制少量漂白粉。
现已知反应:2Cl2+2Ca(OH)2==Ca(ClO)2+CaCl2+2H2O
温度稍高即发生副反应:6Cl2+6Ca(OH)2==Ca(ClO3)2+5CaCl2+6H2O
现有三个同学分别设计的三套实验装置如下:

(1)请从①不容易控制反应速率,②容易控制反应速率,③有副反应发生,④可防止副反应发生,⑤污染环境,⑥可防止污染环境几个方面对上述甲、乙、丙三套装置的优缺点作出评析,并选择符合题目要求的选项填在空格内。
| 优点 | 缺点 |
甲装置 |
|
|
乙装置 |
|
|
丙装置 |
|
|
(2)上述装置中,甲由A、B两部分组成,乙由C、D、E三部分组成,丙由F、G两部分组成。请从上述装置中,选取合理的组成部分,组装一套较完善的实验装置,装置各部分的连接顺序(按气流从左到右的方向)是________________________。
(3)实验中若用12 mol·L-1的浓盐酸100 mL与足量的MnO2反应,最终生成Ca(ClO)2的物质的量_______________0.15 mol(填“大于”“小于”或“等于”),其原因是____________(假定各步反应均无反应物损耗,且无副反应发生)。
查看答案和解析>>
科目:高中化学 来源: 题型:
A.Cl2 B.KMnO4 C.FeCl3 D.HCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com