
【题目】常温下,Ka (HCOOH)=1.77×10-4,Ka (CH3COOH)=1.75×10-5,Kb (NH3·H2O) =1.76×10-5,下列说法正确的是( )
A. 将CH3COONa溶液从20℃升温至30℃,溶液中 增大
增大
B. 用相同浓度的NaOH溶液分别滴定等体积pH均为3的HCOOH和CH3COOH溶液至终点,消耗NaOH溶液的体积相等
C. 0.2 mol/L HCOOH 与 0.1 mol/L NaOH 等体积混合后:c(HCOO-) + c(OH-) = c(HCOOH) + c(H+)
D. 0.2 mol/L CH3COONa 与 0.1 mol/L盐酸等体积混合后 (pH<7):c(CH3COO-) > c(Cl- ) >c(CH3COOH) >c(H+)
【答案】D
【解析】CH3COONa的水解过程为吸热,所以升高温度,平衡右移,水解平衡常数c(OH-) ×c(CH3COOH) /c(CH3COO-)增大,溶液中 减小,A错误;pH相同的HCOOH和
减小,A错误;pH相同的HCOOH和![]() ,浓度:
,浓度:![]() ,用相同浓度的NaOH溶液分别滴定等体积pH均为3的HCOOH和
,用相同浓度的NaOH溶液分别滴定等体积pH均为3的HCOOH和![]() 溶液至终点时,酸的浓度越大,消耗的碱体积越大,pH、体积相同的HCOOH和
溶液至终点时,酸的浓度越大,消耗的碱体积越大,pH、体积相同的HCOOH和![]() ,物质的量前者小于后者,所以后者消耗的NaOH体积多,B错误;两溶液等体积混合后得到甲酸和甲酸钠溶液,由电荷守恒c(H+)+c(Na+)=c(OH-)+c(HCOO-)和物料守恒2c(Na+)=c(HCOOH)+c(HCOO-)可得c(HCOO-) + 2c(OH-) = c(HCOOH) + 2c(H+),C项错误;二者混合后溶液中的溶质为等物质的量浓度的
,物质的量前者小于后者,所以后者消耗的NaOH体积多,B错误;两溶液等体积混合后得到甲酸和甲酸钠溶液,由电荷守恒c(H+)+c(Na+)=c(OH-)+c(HCOO-)和物料守恒2c(Na+)=c(HCOOH)+c(HCOO-)可得c(HCOO-) + 2c(OH-) = c(HCOOH) + 2c(H+),C项错误;二者混合后溶液中的溶质为等物质的量浓度的![]() 、
、![]() 和NaCl,混合溶液的
和NaCl,混合溶液的![]() ,说明醋酸电离程度大于醋酸钠水解程度,乙酸是弱酸,其电离程度较小,所以粒子浓度大小顺序是c(CH3COO-) > c(Cl- ) >c(CH3COOH) >c(H+);D正确;正确选项D。
,说明醋酸电离程度大于醋酸钠水解程度,乙酸是弱酸,其电离程度较小,所以粒子浓度大小顺序是c(CH3COO-) > c(Cl- ) >c(CH3COOH) >c(H+);D正确;正确选项D。


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】实验室里用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)来制备绿矾(FeSO4·7H2O)和聚铁(碱式硫酸铁的聚合物),其过程如下:

(1)若用浓硫酸配制过程①所需的250mL3.0mol·L-1的稀硫酸,所用的玻璃仪器除烧杯、玻璃棒和量筒外,还需要_____。
(2)过程②用到多种硅酸盐质的仪器,除玻璃棒、酒精灯、泥三角外,还有_____(填仪器名称),该过程产生的尾气会对大气造成污染,可选用下列试剂中的_____吸收。
a.浓硫酸 b.蒸馏水 c.NaOH溶液 d.浓硝酸
(3)过程③中,需要加入的物质名称是____,检验溶液X中金属阳离子是否完全转化的试剂为_____(填试剂名称)。
(4)过程④的操作是将溶液______、_____、过滤、洗涤,即得到FeSO4·7H2O晶体。过程⑥中,将溶液Z加热到70~80℃,目的是__。
(5)实验室为测定所得到的聚铁样品中铁元素的质量分数,进行下列实验。①用分析天平称取样品2.700g;②将样品溶于足量盐酸后,加入足量的氯化钡溶液;③过滤、洗涤、干燥、称量,得固体质量为3.495g。若该聚铁主要成分为[Fe(OH)SO4]n,则该聚铁中铁元素的质量分数为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将由NaOH、BaCl2、Al2(SO4)3三种固体组成的混合物溶于足量的水中,充分溶解后,向混合溶液中滴加1mol·L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的质量关系如图所示。下列有关判断正确的是( )
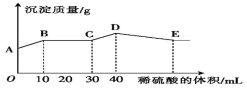
A.AB段发生反应的离子方程式为Ba2++SO42-=BaSO4↓
B.BC段发生反应的离子方程式为H++OH-=H2O
C.D点表示的沉淀的化学式为Al(OH)3
D.E点时溶液中含有大量的AlO2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢卤酸的能量关系如图所示:下列说法正确的是( )
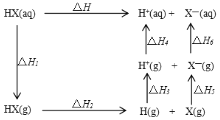
A.已知HF气体溶于水放热,则HF的△H1<0
B.相同条件下,HCl的△H2比HBr的小
C.相同条件下,HCl的(△H3+△H4)比HI的大
D.已知△H>0,对于HF和HCl,都有△H1+△H2>-(△H3+△H4+△H5+△H6)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知同温同压下,下列反应的焓变和平衡常数分别表示如下,有关说法正确的是( )
(1)2SO2(g)+O2(g) ![]() 2SO3(g) △Hl=-197 kJ/mol K1=a
2SO3(g) △Hl=-197 kJ/mol K1=a
(2)2NO(g)+O2(g) ![]() 2NO2(g) △H2=-144 kJ/mol K2=b
2NO2(g) △H2=-144 kJ/mol K2=b
(3)NO2(g)+SO2(g) ![]() SO3(g)+NO(g) △H3=m kJ/mol K3=c
SO3(g)+NO(g) △H3=m kJ/mol K3=c
A. m=26.5 c2= a/b B. m--26.5 2c=a-b C. m=-170.5 2c=a-b D. m=53 c2=a/b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将浓度均为0.1mol/L、体积不同的HA溶液与BOH 溶液混合,保持溶液的总体积为100 mL,溶液的体积与混合液pH 的关系如图所示。下列说法正确的是

A. V1表示HA 溶液的体积,V2表示BOH 溶液的体积
B. Ka( HA) 和Kb( BOH) 的数量级相等,均为10-6
C. y点时,c(B+)=c(A-)=c(OH-)=c(H+)
D. x、y、z 所示三点时水的电离程度:y>x=z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验现象与实验操作不相匹配的是
实验操作 | 实验现象 | |
A | 向盛有高锰酸钾酸性溶液的试管中通入足量的乙烯后静置 | 溶液的紫色逐渐褪去,静置后溶液分层 |
B | 将镁条点燃后迅速伸入集满CO2的集气瓶 | 集气瓶中产生浓烟并有黑色颗粒产生 |
C | 向盛有饱和硫代硫酸钠溶液的试管中滴加稀盐酸 | 有刺激性气味气体产生,溶液变浑浊 |
D | 向盛有FeCl3溶液的试管中加过量铁粉,充分振荡后加1滴KSCN溶液 | 黄色逐渐消失,加KSCN后溶液颜色不变 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钒钛磁铁矿炼钢后剩余的尾渣中含有V2O3、MgO、Al2O3、Fe2O3、SiO2等,现从该
钒渣中回收V2O3的工艺流程如下:
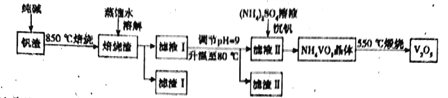
(1)滤液I的成分是NaVO3、NaAlO3和_________(写化学式)。
(2)检验滤渣I中是否含有Fe2O3的方法是_________________。
(3)用离子方程式表示NaAlO3溶液具有碱性的原因_________________。
(4)加入硫酸铵溶液后溶液的pH会有所降低,已知常温时氨水的电离平衡常数Kb=2×10-5;则0.1 mol·L-1 (NH4)2SO4溶液的PH约为__________。
(5)在沉钒操作中,选择使用(NH4)2SO4比使用(NH4)2CO3的沉钒效率高,其原因为___________。
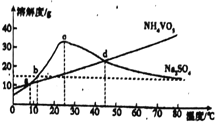
(6)NH4VO3和Na2SO4的混合液需要经过蒸发浓缩、趁热过滤、冷却结晶和过滤等操作得到NH4VO3晶体,结合下图,分析为了得到较纯净的NH4VO3晶体和较高的晶体析出率,应选择最适宜的结晶温度,为a、b、c、d四点中______点对应的温度。
(7)最后制备V2O3时煅烧的温度不宜过高,当温度在1000℃时,偏钒酸铵(NH4VO3)会分解生成V2O3>和N2以及其他常见的氧化物,请写出偏钒酸铵在1000℃时分解的化学方程式:___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论不正确的是
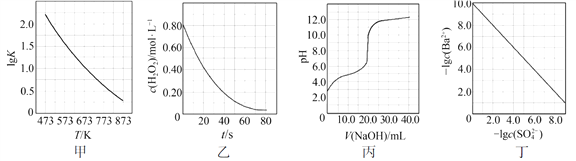
A. 图甲是CO(g)+H2O(g)![]() CO2(g)+H2(g)的平衡常数与反应温度的关系曲线,说明该反应的ΔH<0
CO2(g)+H2(g)的平衡常数与反应温度的关系曲线,说明该反应的ΔH<0
B. 图乙是室温下H2O2催化分解放出氧气的反应中c(H2O2 )随反应时间变化的曲线,说明随着反应的进行H2O2分解速率逐渐减小
C. 图丙是室温下用0.1000 mol·L1NaOH溶液滴定20.00 mL 0.1000 mol·L1某一元酸HX的滴定曲线,说明HX是一元强酸
D. 图丁是室温下用Na2SO4除去溶液中Ba2+达到沉淀溶解平衡时,溶液中c(Ba2+ )与c(SO42)的关系曲线,说明溶液中c(SO42 )越大c(Ba2+ )越小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com