
����Ŀ������100ml 0.5molL��1Na2CO3��Һ����Na+Ũ��Ϊ0.20molL��1����Һ�����в�����ȷ���ǣ� ��
A.����Na2CO3 ��Һת����250ml����ƿ�У�������ˮϡ�����̶��ߣ�ҡ��
B.����Na2CO3 ��Һת����250ml�ձ��У�����Ͳ��ȡ150ml����ˮ���룬����
C.����Na2CO3 ��Һת����250ml�ձ��У�����Ͳ��ȡ400ml����ˮ���룬����
D.����Na2CO3 ��Һת����500ml����ƿ�У�������ˮϡ�����̶��ߣ�ҡ��
���𰸡�D
�������� �⣺A������ƿ������Ϊϡ����������һ�ֶ�����������A����
B������ϡ��ǰ�������ӵ����ʵ������ֲ��䣬������Ҫ��Һ�����Ϊ�� ![]() mL=500mL������Һ������Ӧ������ƿ�н��У��������ձ��У���B����
mL=500mL������Һ������Ӧ������ƿ�н��У��������ձ��У���B����
C������һ�����һ��Ũ�ȵ���ҺҪʹ������ƿ�����ݣ��������ձ��н��У���100mL��̼������Һ����400mLˮ֮��������Һ�������һ����500mL����C����
D������ϡ��ǰ�������ӵ����ʵ������ֲ��䣬������Ҫ��Һ�����Ϊ�� ![]() mL=500mL��Ҫʹ��500mL������ƿ����D��ȷ��
mL=500mL��Ҫʹ��500mL������ƿ����D��ȷ��
��ѡD��
�����㾫����������Ĺؼ������������ʵ���Ũ�ȵĸ�������֪ʶ�������Ե�λ�������������B�����ʵ�������ʾ��Һ��ɵ�����������������B�����ʵ���Ũ�ȣ�����CB=nB(mol)��V(L) ��nB������B�����ʵ�����V����Һ���������λ��mol��L��1��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Cl2��H2O2�Ǹ��н����������������������������Cl2��������ǿ��H2O2 �� �ܽ�H2O2������Ϊ����֤ijС��ѧ�����������ͼ��ʾ��ʵ��װ�ý���ʵ�飨�г�װ����ȥ����
��֪��2KMnO4+16HCl(Ũ) = 2KCl + 2MnCl2 + 5Cl2�� + 8H2O
�Թ�B�б���ʳ��ˮ����Ҫ�����dz�ȥCl2�л��е�HCl
��ش��������⡣
��1���Թ�C������Ӧ�Ļ�ѧ����ʽ����
��2���Թ�D��NaOH��Һ����������
��3����Ũ����ע��Բ����ƿA����װ���еĿ��������ž���ر�D��ֹˮ�У���Ӧһ��ʱ����Թ�D�е�����Ϊ �� �Թ�D�е�������鷽��Ϊ��
��4���е�ͬѧ������ʵ����D�Թ��е�������Դ�������ɣ�����Ϊ���ܵ���Դ�����÷���ʽ�ش�)���������ɿ��Բ��öԱ�ʵ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�����ڱ���ѧϰ��ѧ����Ҫ���ߣ���������������Ϣ���ɣ��±����������ֶ����ڵ�ԭ�Ӱ뾶����Ҫ���ϼۣ���֪���ԭ�Ӱ뾶Ϊ0.089nm����
Ԫ�ش��� | A | B | C | D | E |
ԭ�Ӱ뾶/nm | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 |
��Ҫ���ϼ� | +2 | +3 | +6����2 | ��1 | ��2 |
��1����Ԫ�ش��ű�����������ڱ��ж�Ӧλ�ã�����Ϊ���ڱ���һ���֣��� 
��2��BԪ�ش���Ԫ�����ڱ��������壻
��3����Ԫ�����ڱ����ķֽ紦�������ҵ��ư뵼����ϵ�Ԫ�أ�
��4����������Ԫ�ص�����������Ӧˮ������������ǿ�������ѧʽ����
��5��C��E�γɵĻ�����M����ʹ���Ը��������Һ��ɫ��������M���ԣ�
��6��д��D��ǿ����Һ��Ӧ�����ӷ���ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Դ��һ����Ҫ�������Դ���������ֿɲ���H2�Ļ�������ң���6.00g��������ȫ�ֽ⣬ֻ�õ�һ�ֶ�����Ԫ�صĽ������ʺ�6.72L��H2��������ɱ�״����������ˮ��ӦҲ�ܷų�H2 �� ͬʱ������һ�ְ�ɫ������ð�ɫ����������NaOH��Һ�����������ڴ��������¿ɷֽ�õ�H2����һ�ֵ�������������ڱ�״���µ��ܶ�Ϊ1.25gL��1 �� ��ش��������⣺
��1���Ļ�ѧʽ�� ��
��2������ˮ��Ӧ�Ļ�ѧ����ʽ�� ��
��3������������þ��Ӧ�IJ��������û�ѧʽ��ʾ����
��4�����ڼ�����������CuO��Ӧ������Cu���������д���÷�Ӧ�Ļ�ѧ����ʽ �� �����������Cu�п��ܻ�����Cu2O�������ʵ�鷽����֤����֪��Cu2O+2H+�TCu+Cu2++H2O��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڰ뵼�幤ҵ�У���һ����������⡣����Ĺ���������ͼ��ʾ��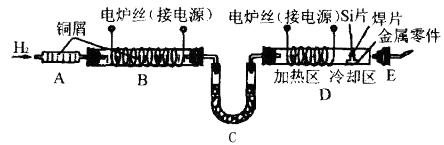
����ʱ���ǽ�ʯӢ��D���ڴ�������ȼ���뵼���Ƭ����Ƭ�ͽ��������ʯӢ�ܿ��������������������ԭ�����м���ʹ��Ƭ�ۻ�������������������������һ�𡣺��Ӻ��ٽ����������ȴ������ȴ��ȡ����������е���������Ҫ�ߣ���ҵ�����京������99.9�������Ժ��м�����ˮ���������������Ե�ȼ����ǰӦ���������Ĵ��ȡ��Իش��������⣺
��1��װ��B����������B�з�����Ӧ�Ļ�ѧ����ʽ����
��2��װ��C�е���������C����������
��3����ȼ����ǰ��E�������ܽ���������D���ڴ���Ŀ������
��4��װ��A�ǰ�ȫƿ�����Է�ֹ����ȼ�ջػ�����ը��������������ͭм����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ������У�����������������( )
A. �������з���NaCl��Һ�����ȡ������õ�NaCl����
B. ��10 mL����Ͳ��ȡ9.20 mL������
C. ��������ƽ��ȡ5.00 g NaCl
D. ��500 mL����ƿ����450 mL 0.1 mol��L��1������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��pHֵΪ3��CH3COOH��pHΪ11��NaOH��Һ�������ϣ���Ϻ���ҺpHΪ�� ��
A.pH��7
B.pH��7
C.pH=7
D.���ж�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��һЩ��Ҫ��ҵ������ת����ϵ����Ӧ������ȥ����������������⣺ 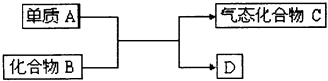
��1����D�ǵ��ʣ�����A����ͬһ���壬��Ӧ�ڸ����½��У��� �ٴ˷�Ӧ�Ļ�ѧ����ʽ�� ��
��D���ʵ�һ����Ҫ��;�� ��
��2����BΪ��ɫ���壬DΪ���廯�����÷�ӦΪ4FeS2+11O2 ![]() 2Fe2O3+8SO2�ٵ���1molC����ʱ���÷�Ӧת�Ƶ��ӵ������� ��
2Fe2O3+8SO2�ٵ���1molC����ʱ���÷�Ӧת�Ƶ��ӵ������� ��
�ڽ�Cͨ������������KMnO4 ��Һ�У�������Ӧ�����ӷ���ʽΪ ��
��3����B��һ�ּ������壬DΪ������� �ٸ÷�Ӧ�Ļ�ѧ����ʽ�� ��
��B�ڼ�����������CuO��Ӧ��Cu���ɣ��÷�Ӧ�Ļ�ѧ����ʽΪ�������������Cu�п��ܻ�����Cu2O����֪Cu+��������Һ�в����ȶ����ڣ�Ϊ��֤Cu2O�Ƿ���ڣ���ȡ������Ӧ����μ�����ϡ���ᣬ����Һ����ɫ��Ϊ��ɫ����֤������Cu2O����д��������Ӧ�Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����MgCl2��AlCl3�Ļ����Һ������μ���NaOH��Һֱ�����������ⶨ�������NaOH�����ʵ���(mol)�����ó��������ʵ���(mol)�Ĺ�ϵ����ͼ��ʾ��

��1��д���������߶η����ķ�Ӧ�����ӷ���ʽ��
OD��________________________________________________��
DC��________________________________________________��
��2��ԭ��Һ��Mg2����Al3�������ʵ���Ũ��֮��Ϊ________��
��3��ͼ��C���ʾ������______mol NaOHʱ��Al3���Ѿ�ת��Ϊ_____��Mg2���Ѿ�ת��Ϊ______��
��4��ͼ���߶�OA��AB��________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com