
����Ŀ��������ѧ��������ɷ�V��V��Markovnikov��1838��1904��������Գ�ϩ���ļӳɹ���Markovnikov Rule��������������
��֪����CH3CH2Br+NaCN![]() CH3CH2CN+NaBr
CH3CH2CN+NaBr
��CH3CH2CN![]() CH3CH2COOH
CH3CH2COOH
��CH3CH2COOH![]() CH3CHBrCOOH
CH3CHBrCOOH
�������л���֮����ת����

�ش��������⣺
��1��ָ�������л���Ӧ�����ͣ�B��C ��
��2��д�������л���Ӧ�Ļ�ѧ����ʽ��E��F��FΪ�߷��ӻ�����ʱ�� ��
��3��F�����ж��ֽṹ��д�����������F�Ľṹ��ʽ��
�ٷ���ʽΪC7H12O5 ��
�ڷ����ں���һ����Ԫ�� ��
��4��������һ����Ӧ��ѭ���Գ�ϩ���ļӳɹ��� ��
���𰸡���1��ȡ����Ӧ��
��2��n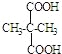 +n HOCH2CH2OH
+n HOCH2CH2OH![]()
![]() +2n H2O��
+2n H2O��
��3����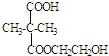 ��
��
��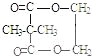 ��
��
��4����ϩ��HBr�ӳ�����A��
��������
������������ݱ�ϩ��CH3CH��CN��CH3��֪A�Ľṹ��ʽΪCH3CHBrCH3����Ϸ�Ӧ��Ϣ�ڿ�֪BΪ��CH3��2CHCOOH����Ϸ�Ӧ��Ϣ�ۿ�֪CΪ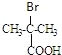 ����Ϸ�Ӧ��Ϣ�ٿ�֪DΪ
����Ϸ�Ӧ��Ϣ�ٿ�֪DΪ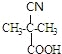 ��EΪ
��EΪ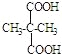 ��E���Ҷ�����Ӧʱ�ɷ���������Ӧ��������Ӧ�ֱ��γ���״������״���߾���γɸ߾���ʱF�Ľṹ��ʽΪ
��E���Ҷ�����Ӧʱ�ɷ���������Ӧ��������Ӧ�ֱ��γ���״������״���߾���γɸ߾���ʱF�Ľṹ��ʽΪ![]() ����F����ʽΪC7H12O5����F�Ľṹ��ʽΪ
����F����ʽΪC7H12O5����F�Ľṹ��ʽΪ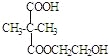 ����F�γ���Ԫ��״������F�Ľṹ��ʽΪ
����F�γ���Ԫ��״������F�Ľṹ��ʽΪ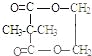 ��
��
�⣺���ݱ�ϩ��CH3CH��CN��CH3��֪A�Ľṹ��ʽΪCH3CHBrCH3����Ϸ�Ӧ��Ϣ�ڿ�֪BΪ��CH3��2CHCOOH����Ϸ�Ӧ��Ϣ�ۿ�֪CΪ ����Ϸ�Ӧ��Ϣ�ٿ�֪DΪ
����Ϸ�Ӧ��Ϣ�ٿ�֪DΪ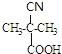 ��EΪ
��EΪ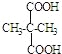 ��E���Ҷ�����Ӧʱ�ɷ���������Ӧ��������Ӧ�ֱ��γ���״������״���߾���γɸ߾���ʱF�Ľṹ��ʽΪ
��E���Ҷ�����Ӧʱ�ɷ���������Ӧ��������Ӧ�ֱ��γ���״������״���߾���γɸ߾���ʱF�Ľṹ��ʽΪ![]() ����F����ʽΪC7H12O5����F�Ľṹ��ʽΪ
����F����ʽΪC7H12O5����F�Ľṹ��ʽΪ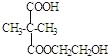 ����F�γ���Ԫ��״������F�Ľṹ��ʽΪ
����F�γ���Ԫ��״������F�Ľṹ��ʽΪ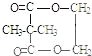 ��
��
��1��B��C�ǣ�CH3��2CHCOOH����ȡ����Ӧ���� ��
��
�ʴ�Ϊ��ȡ����Ӧ��
��2��E��F��FΪ�߷��ӻ�����ʱ���ķ�Ӧ����ʽΪ��n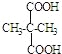 +n HOCH2CH2OH
+n HOCH2CH2OH![]()
![]() +2n H2O��
+2n H2O��
�ʴ�Ϊ��n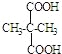 +n HOCH2CH2OH
+n HOCH2CH2OH![]()
![]() +2n H2O��
+2n H2O��
��3��F�����ж��ֽṹ��
��F����ʽΪC7H12O5��ΪE���Ҷ�������������Ӧ�γ���״���õ�����F�Ľṹ��ʽΪ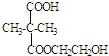 ���ʴ�Ϊ��
���ʴ�Ϊ��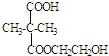 ��
��
��F�����ں���һ����Ԫ����ΪE���Ҷ�������������Ӧ�γɻ�״���õ�����F�Ľṹ��ʽΪ��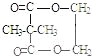 ���ʴ�Ϊ��
���ʴ�Ϊ��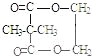 ��
��
��4����ϩ���ǶԳƽṹ��ϩ������ϩ��HBr�ӳ�����A�ķ�Ӧ��ѭ���Գ�ϩ���ļӳɹ���
�ʴ�Ϊ����ϩ��HBr�ӳ�����A��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������11�����Ӻ�10�����ӵ�������
A. Na�� B. O2�D C. Mg2�� D. F�D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼���(NH4)2CO3�������¾����Է��ķֽ��������������˵����ȷ����( )
A��̼��立ֽ�����Ϊ�������ӷ������壬ʹ��ϵ��������
B��̼��立ֽ�����Ϊ������������
C��̼��立ֽ������ȷ�Ӧ�����������оݲ����Է��ֽ�
D��̼���ζ����ȶ��������Է��ֽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ��ơ�ɳ�ӣ���Ҫ�ɷ�ΪSiO2)��������������ɵĹ���������룬���ѧ�IJ���˳���ǣ� ��
A���ܽ⡢���ˡ����ȣ����������������ᾧ��
B�����ȣ����������ܽ⡢���ˡ��������ᾧ��
C�����ȣ����������ܽ⡢���ᾧ
D���ܽ⡢�ᾧ�����ˡ����ȣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���̶�������ܱ������У�����2mol A��1mol B�������·�Ӧ��2A��g��+B��g��![]() 3C��g��+D��g�����ﵽƽ��ʱ��C��Ũ��ΪW mol/L����ά������������¶Ȳ��䣬���������ַ����ı���ʼ���ʣ��ﵽƽ���C��Ũ����ΪW mol/L����
3C��g��+D��g�����ﵽƽ��ʱ��C��Ũ��ΪW mol/L����ά������������¶Ȳ��䣬���������ַ����ı���ʼ���ʣ��ﵽƽ���C��Ũ����ΪW mol/L����
A��4molA+2molB B��1��5molC+0��5molD
C��1molB+1molD D��1molA+0��5molB+1��5molC+0��5molD
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ֻ��һ���Լ��Ϳ��Լ���������Һ����������Һ��������Һ�������Լ���( )
A��NaOH��Һ B������Cu(OH)2����Һ C��ʯ����Һ D��Na2CO3��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ������Fe��Fe2O3�����Ͷ��2mol/L250mL��HNO3��Һ�У���Ӧ��ȫ������ʣ�࣬����2.24L����״����NO���壬����Ӧ����Һ�м���1mol/L��NaOH��Һ��Ҫʹ��Ԫ��ȫ����������������NaOH��Һ����������ǣ� ��
A��400mL B��450mL C��500mL D����ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D����Ԫ�أ�ԭ��������������Aԭ�ӵ����������4�����ӣ�B�������Ӻ�C�������Ӿ�����ͬ�ĵ��Ӳ�ṹ����Ԫ�صĵ��ʷ�Ӧ������һ�ֵ���ɫ�Ĺ���E��D��L�����������K��M�������Ӳ��ϵĵ�����֮�ͣ�
��1��AΪ ��BΪ ��CΪ ��D ������д��Ӧ��Ԫ�����ƣ�
��2��д����C��D��Ԫ����ɵĻ�����ĵ���ʽ ��
��3��A�����������ĵ���ʽ ��C�����������ˮ����ĵ���ʽ ������ɫ�Ĺ���E�ĵ���ʽ ��
��4��д��A��B�Ļ�������E��Ӧ�Ļ�ѧ����ʽ�� ��
��5��д��DԪ�ص�����������ˮ�����A�ĵ��ʷ�Ӧ�Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����10L�����ܱ������г���X(g)��Y(g)��������ӦX(g)��Y(g)![]() M(g)��N(g)������ʵ���������±���
M(g)��N(g)������ʵ���������±���
ʵ�� | �¶�/��[ | ��ʼʱ���ʵ���/mol | ƽ��ʱ���ʵ���/mol[��] | |
n(X) | n(Y) | n(M) | ||
�� | 700 | 0.40 | 0.10 | 0.090 |
�� | 800 | 0.10 | 0.40 | 0.080 |
�� | 800 | 0.20 | 0.30 | a |
�� | 900 | 0.10 | 0.15 | b |
����˵����ȷ���ǣ� ��
A��ʵ�����У���5minʱ���n(M)��0.050mol����0��5minʱ���ڣ���N��ʾ��ƽ����Ӧ����v(N)��2.0��10��2mol/(L��min)
B��ʵ�����У��÷�Ӧ��ƽ�ⳣ��K��2.0
C��ʵ�����У��ﵽƽ���ǣ�X��ת����Ϊ60%
D��ʵ�����У��ﵽƽ��ʱ��b��0.060
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com