
| A. | Cl-、Cu2+、SO42-、NO3- | B. | Cl-、Na+、SO42-、CH3COO- | ||
| C. | Cl-、Fe2+、MnO4-、NO3- | D. | AlO2-、Na+、SO42-、NO3- |
分析 透明强酸性溶液中存在大量氢离子,
A.四种离子之间不反应,都不与氢离子反应;
B.醋酸根离子与氢离子反应生成弱电解质醋酸;
C.酸性条件下硝酸根离子、高锰酸根离子能够氧化亚铁离子;
D.偏铝酸根离子与氢离子反应.
解答 解:A.Cl-、Cu2+、SO42-、NO3-之间不反应,都不与氢离子反应,在溶液中能够大量共存,故A正确;
B.CH3COO-与强酸性溶液中的氢离子反应,在溶液中不能大量共存,故B错误;
C.Fe2+与MnO4-、NO3-发生氧化还原反应,在溶液中不能大量共存,故C错误;
D.AlO2-与强酸性溶液中的氢离子反应,在溶液中不能大量共存,故D错误;
故选A.
点评 本题考查离子共存,为高考的高频题,题目难度中等,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.


科目:高中化学 来源: 题型:选择题
| A. | 原子最外层电子数:X>Y>Z | B. | 原子半径:X>Y>Z | ||
| C. | 离子半径:X2->Y+>Z- | D. | 原子序数:X>Y>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
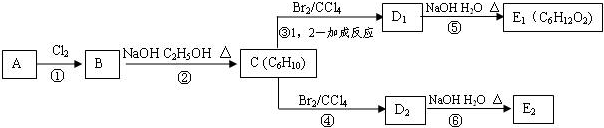
 ;E2含有的含氧官能团的名称为:羟基.
;E2含有的含氧官能团的名称为:羟基.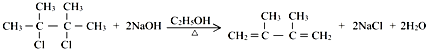 ,反应类型为:消去反应;反应⑥的化学方程式为:
,反应类型为:消去反应;反应⑥的化学方程式为: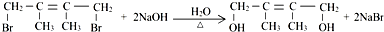 ,反应类型为:水解反应(或取代反应).
,反应类型为:水解反应(或取代反应).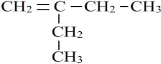 、
、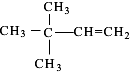 (均不考虑立体异构).
(均不考虑立体异构).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+、K+、SO42-、Cl-、Al[(OH)4]- | B. | Al3+、Na+、Cl-、SO42-、NO3- | ||
| C. | Na+、K+、SO42-、NO3-、Cl- | D. | Fe2+、H+、Br-、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
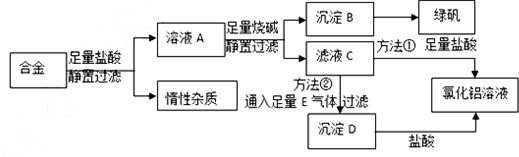
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色气体,难溶于水,密度比空气略小 | |
| B. | 乙烯燃烧时,火焰明亮,同时产生黑烟 | |
| C. | 与溴水发生取代反应而使溴水褪色 | |
| D. | 乙烯的产量标志着一个国家的石油化工水平 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子晶体中只含有离子键,不含有共价键 | |
| B. | 水分子很稳定,因为水分子间存在氢键 | |
| C. | 分子晶体中一定存在分子间作用力,不一定存在共价键 | |
| D. | I的原子半径大于Br,HI比HBr的热稳定性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

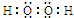 ;Ⅰ中发生反应的还原剂是Na2SO3(填化学式).
;Ⅰ中发生反应的还原剂是Na2SO3(填化学式).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com