
已知X、Y是主族元素,I为电离能,单位是kJ·mol-1。请根据下表所列数据判断,错误的是( )
| 元素 | I1 | I2 | I3 | I4 |
| X | 500 | 4 600 | 6 900 | 9 500 |
| Y | 580 | 1 800 | 2 700 | 11 600 |
A.元素X的常见化合价是+1
B.元素Y是ⅢA族元素
C.元素X与氯形成化合物时,化学式可能是XCl
D.若元素Y处于第3周期,它可与冷水剧烈反应
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:
逻辑推理是化学学习中常用的一种思维方法,以下四个推理中正确的是( )
A.有机物一定含有碳元素,所以含碳元素的化合物一定是有机物
B.置换反应一定生成一种
C.含碳元素的物质在O2中充分燃烧会生成CO2,所以在O2中燃烧能生成CO2的物质一定含碳元素
D.盐的组成中含有金属阳离子与酸根离子,所以盐中一定不含氢元素
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,在一容积可变的容器里,反应2A(g) B(g)+2C(g)达到平衡时,A、B和C的物质的量分别为4 mol、2 mol、4 mol。在保持温度和压强不变的条件下,下列说法正确的是( )
B(g)+2C(g)达到平衡时,A、B和C的物质的量分别为4 mol、2 mol、4 mol。在保持温度和压强不变的条件下,下列说法正确的是( )
A.充入1 mol 稀有气体氦(He),平衡不移动
B.充入A、B、C各1 mol,平衡将向正反应方向移动
C.将A、B、C各物质的量都减半,C的百分含量不变
D.加入一定量的A气体达到平衡后,C的百分含量一定增加
查看答案和解析>>
科目:高中化学 来源: 题型:
现有常温下的六份溶液:
①0.01 mol·L-1CH3COOH溶液;
②0.01 mol·L-1HCl溶液;
③pH=12的氨水;
④pH=12的NaOH溶液;
⑤0.01 mol·L-1CH3COOH溶液与pH=12的氨水等体积混合后所得溶液;
⑥0.01 mol·L-1HCl溶液与pH=12的NaOH溶液等体积混合所得溶液。
(1)其中水的电离程度最大的是 (填序号,下同),水的电离程度相同的是 ;
(2)若将②、③混合后所得溶液pH=7,则消耗溶液的体积:② ③(填“>”“<”或“=”);
(3)将六份溶液同等稀释10倍后,溶液的pH:
① ②,③ ④,⑤ ⑥(填“>”“<”或“=”);
(4)将①、④混合,若有c(CH3COO-)>c(H+),则混合溶液可能呈 (填序号)。
A.酸性 B.碱性 C.中性
查看答案和解析>>
科目:高中化学 来源: 题型:
在周期表主族元素中,甲元素与乙、丙、丁三种元素紧密相邻。这四种元素原子的最外层电子数之和为20;甲、丁的原子序数之和比乙、丙的原子序数之和大10;乙的原子序数小于丙。下列判断中不正确的是( )
A.甲的某种单质与丙的单质均可形成正四面体空间结构
B.四种原子半径:丙>乙>甲>丁
C.甲、乙、丙、丁四种单质的熔点最低的是乙
D.乙的氢化物与丁的氢化物能相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关等离子体的说法中,不正确的是( )
A.等离子体内部全部是带电荷的微粒
B.等离子体中正、负电荷大致相等
C.等离子体具有很好的导电性
D.等离子体用途十分广泛
查看答案和解析>>
科目:高中化学 来源: 题型:
下列评价及离子方程式书写正确的是( )
| 选项 | 离子组 | 评价 |
| A | H+、Fe2+、 | 不能大量共存于同一溶液中,因为发生了氧化还原反应4Fe2++2 |
| B | Na+、 | 不能大量共存于同一溶液中,因为有沉淀生成2Al3++3 |
| C |
| 能大量共存于同一溶液中 |
| D |
| 不能大量共存于同一溶液中,因为发生如下反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对分子的性质的解释中,不正确的是
A.水很稳定(1000℃以上才会部分分解)是因为水中含有大量的氢键所致
B.乳酸(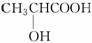 )有一对手性异构体,因为其分子中含有一个手性碳原子
)有一对手性异构体,因为其分子中含有一个手性碳原子
C.碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释
D.酸性:H3PO4>HClO,因为H3PO4的非羟基氧原子数比HClO的多
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com