
| A、①中水的电离程度最小,③中水的电离程度最大 |
| B、将②、③混合,若pH=7,则消耗溶液的体积:②>③ |
| C、将①、④混合,若c(CH2COO-)>c(H+),则混合液一定呈碱性 |
| D、将四份溶液分别稀释100倍后,溶液的pH:③>④,①<② |


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
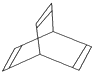 有机物的结构可用“键线式”简化表示,如:CH3-CH=CH-CH3可表示为
有机物的结构可用“键线式”简化表示,如:CH3-CH=CH-CH3可表示为 ,有一种有机物X的键线式如图所示.
,有一种有机物X的键线式如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:

 ②
② ③CH2=CH-CH=CH2 ④
③CH2=CH-CH=CH2 ④
 ⑥
⑥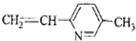
| A、②③⑤ | B、②③⑥ |
| C、①②⑥ | D、②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
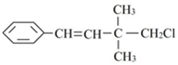
| A、能使酸性KMnO4溶液、溴水褪色,原理相同 |
| B、1 mol该有机物能与H2发生反应,消耗H2 4mol |
| C、一定条件下,能发生加聚反应 |
| D、该有机物苯环上的一个H被取代,有3种同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、镭位于周期表中第七周期ⅡA族 |
| B、镭的硫酸盐难溶于水 |
| C、镭的碳酸盐可溶于水 |
| D、镭的氢氧化物为强碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在镀件上电镀锌时,阳极的电极反应式为:Zn-2e-═Zn2+ |
| B、钢铁发生电化学腐蚀时,正极的电极反应式为:Fe-3e-═Fe3+ |
| C、氯碱工业电解饱和食盐水时,阴极的电极反应式:2Cl--2e-═Cl2↑ |
| D、氢氧燃料电池中电解质为硫酸时,正极的电极反应式为:O2+2H2O+4e-═4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2S和SO2 |
| B、NO和O2 |
| C、NH3和HCl |
| D、Cl2和H2S |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com