
| A.是离子化合物,含有离子键和共价键 |
B.电子式是 |
| C.与水反应时,是还原剂 |
| D.固体投入少量的水中,有两种气体产生 |
 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源:不详 题型:单选题
| 23595 |
| 23592 |
| A.具有相同的原子序数 | B.具有相同的中子数 |
| C.具有相同的质量数 | D.具有相同的核外电子数 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.有些物质是由原子直接构成,如水晶、金刚砂等;有些物质是由分子直接构成,如干冰、明矾等;有些物质是由离子直接构成的,如皓矾、芒硝等 |
| B.BF3、H2O、SiCl4、PCl5四种分子中所有原子都满足最外层8电子结构 |
| C.非金属氧化物不都是酸性氧化物;金属氧化物不都是碱性氧化物 |
| D.尿素的熔点比醋酸的熔点高,这是由于前者比后者有更大的范德华力所致 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.键的极性N—H比P—H强 |
| B.分子的极性NH3比PH3强 |
| C.相对分子质量PH3比NH3大 |
| D.NH3分子之间存在特殊的分子间作用力 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
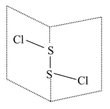
| A.S2Cl2为共价化合物 |
| B.S2Cl2只含有极性共价键 |
| C.S2Cl2与水反应时S—S键和S—Cl键都断裂 |
| D.S2Cl2分子中S—S键和S—Cl键是通过共用电子对的相互作用形成的 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Li3BN2H8。下列有关说法正确的是
Li3BN2H8。下列有关说法正确的是| A.B的原子半径小于N的原子半径 |
| B.H2的结构式为H—H |
| C.放氢过程为化合反应 |
| D.储氢过程没有能量变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.含有NH4+和H- |
| B.NH5中N元素的化合价为+5价 |
| C.1 mol NH5中含有5NA个N—H键 |
| D.与乙醇反应时,NH5被还原 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.该物质为离子晶体 |
| B.该物质可通过C60吸附N2直接制得 |
| C.18g该物质完全分解产生13.44LN2 |
| D.C(N3)4中碳元素为正价 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com