
| A. | 7.8gNa2O2与CO2反应,转移的电子数为0.2NA | |
| B. | 1mol/L的CaCl2溶液中含Cl-的数目为2 NA | |
| C. | 常温常压下,17g NH3含氢原子数目为3NA | |
| D. | 1mol氢氧根离子中含有的电子数为9NA |
分析 A、求出过氧化钠的物质的量,然后根据过氧化钠与二氧化碳的反应为歧化反应来分析;
B、溶液体积不明确;
C、求出氨气的物质的量,然后根据1mol氨气中含3mol氢原子来分析;
D、氢氧根中含10个电子.
解答 解:A、7.8g过氧化钠的物质的量为0.1mol,而过氧化钠与二氧化碳的反应为歧化反应,故0.1mol过氧化钠与二氧化碳反应转移0.1mol电子即0.1NA个,故A错误;
B、溶液体积不明确,故溶液中的氯离子的个数无法计算,故B错误;
C、17g氨气的物质的量为1mol,而1mol氨气中含3mol氢原子,故为3NA个,故C正确;
D、氢氧根中含10个电子,故1mol氢氧根中含10mol电子即10NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:解答题
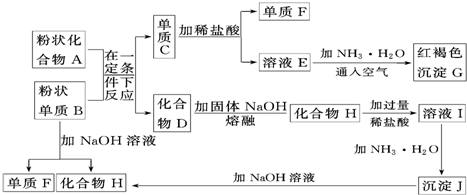
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
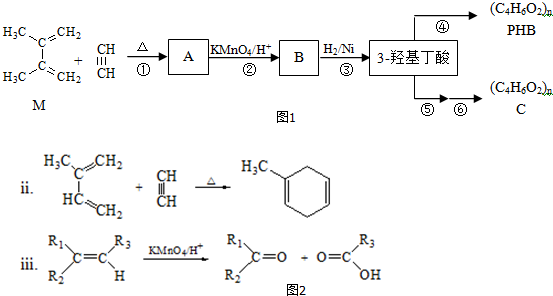
 .
. ;
;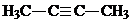 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25% | B. | 80% | C. | 10% | D. | 20% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电离时能够产生H+的化合物是酸 | |
| B. | 难溶的物质(如CaCO3)不能发生离子反应 | |
| C. | 电解质在水中不一定能导电,在水中导电的化合物不一定是电解质 | |
| D. | 胶体加入电解质可产生沉淀,而溶液不能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液氨常被用作制冷剂 | |
| B. | 可利用2Fe3++Cu═Cu2++2Fe2+腐蚀印刷电路板 | |
| C. | 为便于储存和使用,可用液氯代替氯水漂白干燥棉布上的有色物质为便于储存和使用,可用液氯代替氯水漂白干燥棉布上的有色物质 | |
| D. | 已知3Cl2+2NH3═N2+6HCl,工业上可用浓氨水检查氯气管道是否漏气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com