
【题目】有机物G(1,4—环己二醇)是重要的医药中间体和新材料单体,可通过以下流程制备。

完成下列填空:
(1)写出A中官能团名称___。
(2)反应类型:反应①____;反应③____。
(3)写出B的结构简式___。
(4)一定条件下E脱氢反应得一种产物,化学性质比较稳定,易取代、难加成。该产物的结构简式为____。
(5)写出C→G的化学方程式____。
【答案】溴原子 消去反应 取代反应 ![]()
![]()
![]() +2NaOH
+2NaOH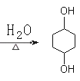 +2NaBr
+2NaBr
【解析】
![]() (D)在浓硫酸、加热条件下发生消去反应,生成
(D)在浓硫酸、加热条件下发生消去反应,生成![]() (E),
(E),![]() 与Br2发生加成反应生成A为
与Br2发生加成反应生成A为![]() ,
,![]() 在NaOH醇溶液中加热,发生消去反应生成
在NaOH醇溶液中加热,发生消去反应生成![]() (F),
(F),![]() 与Br2发生1,4加成,生成B为
与Br2发生1,4加成,生成B为![]() ,
,![]() 与H2发生加成反应生成C为
与H2发生加成反应生成C为![]() ,
,![]() 在NaOH水溶液中发生水解反应生成
在NaOH水溶液中发生水解反应生成![]() (G)。
(G)。
(1)上以上分析知,A的结构简式为![]() ,A中官能团名称溴原子。答案为:溴原子;
,A中官能团名称溴原子。答案为:溴原子;
(2)反应①为![]() 在浓硫酸、加热条件下反应生成
在浓硫酸、加热条件下反应生成![]() ,发生消去反应;反应③为
,发生消去反应;反应③为![]() 在NaOH水溶液中反应生成
在NaOH水溶液中反应生成![]() 和NaBr,发生取代反应。答案为:消去反应;取代反应;
和NaBr,发生取代反应。答案为:消去反应;取代反应;
(3)由以上分析知,B的结构简式为![]() 。答案为:
。答案为:![]() ;
;
(4)一定条件下![]() 脱氢反应得一种产物,化学性质比较稳定,易取代、难加成。该产物应不是烯烃,所以应为苯,结构简式为
脱氢反应得一种产物,化学性质比较稳定,易取代、难加成。该产物应不是烯烃,所以应为苯,结构简式为![]() 。答案为:
。答案为:![]() ;
;
(5)由![]() →
→![]() ,应为碱性条件下的水解反应,化学方程式为
,应为碱性条件下的水解反应,化学方程式为![]() +2NaOH
+2NaOH +2NaBr。答案为:
+2NaBr。答案为:![]() +2NaOH
+2NaOH +2NaBr。
+2NaBr。


科目:高中化学 来源: 题型:
【题目】关于 的说法正确的是( )
的说法正确的是( )
A.所有C原子有可能都在同一平面上
B.有7个碳原子可能在同一条直线上
C.该物质属于苯的同系物
D.该物质的核磁共振氢谱显示各峰面积之比为1:2:2:1:1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸又称安息香酸,结构简式为![]() ,有关性质如表所示。苯甲酸可用于合成纤维、树脂、涂料等,也可作为药物或防腐剂使用,有抑制真菌、细菌生长的作用。实验室用高锰酸钾氧化甲苯可制得苯甲酸,相关反应方程式如下:
,有关性质如表所示。苯甲酸可用于合成纤维、树脂、涂料等,也可作为药物或防腐剂使用,有抑制真菌、细菌生长的作用。实验室用高锰酸钾氧化甲苯可制得苯甲酸,相关反应方程式如下:
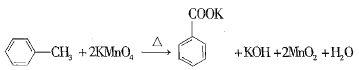
实验时,将一定量的甲苯和高锰酸钾溶液置于图示装置中,在100℃下反应一段时间,再停止反应,并按如下流程分离出苯甲酸和回收未反应的甲苯。
熔点/℃ | 122.4 |
沸点/℃ | 249 |
密度/( | 1.2659 |
水溶性 | 微溶 |
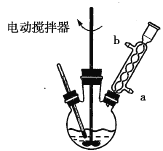
(1)实验中用电动搅拌器进行搅拌的目的是________________。
(2)冷凝管中冷却水是从________(填“a”或“b”)口进入。
(3)操作Ⅰ的名称是,所需的玻璃仪器有________、烧杯;操作Ⅱ的名称是________。
(4)水层用浓盐酸酸化的相关化学方程式为_________________。
(5)如果滤液呈紫色,则要先加入还原剂亚硫酸氢钾,然后再加入浓盐酸酸化,若无此操作会出现的危害是_______________________。
(6)无色液体A的主要成分是________,白色固体B的主要成分是________。
(7)为测定所得产品的纯度,称取1.220g产品,配成![]() 溶液,取其中
溶液,取其中![]() 溶液进行滴定,消耗
溶液进行滴定,消耗![]() 的物质的量为
的物质的量为![]() ,则产品中苯甲酸的质量分数为________。
,则产品中苯甲酸的质量分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是( )。
A.甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种
B.分子式符合![]() 的化合物有6种
的化合物有6种
C.已知二氯苯有3种结构,则四氯苯也有3种结构
D.菲的结构简式为 ,一定条件下,它与硝酸反应,可生成5种一硝基取代物
,一定条件下,它与硝酸反应,可生成5种一硝基取代物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备硝基苯的主要步骤如下:
①配制一定比例的浓硫酸与浓硝酸的混合酸,加入反应器中;
②向室温下的混合酸中逐滴加入一定量的苯,充分振荡;
③在50~60℃下发生反应,直至反应结束;
④除去混合酸后,粗产品依次用蒸馏水和5%![]() 溶液洗涤,最后再用蒸馏水洗涤;
溶液洗涤,最后再用蒸馏水洗涤;
⑤将用无水![]() 干燥后的粗硝基苯进行蒸馏,得到纯硝基苯。
干燥后的粗硝基苯进行蒸馏,得到纯硝基苯。
请回答下列问题:
(1)配制一定比例的浓硫酸与浓硝酸的混合酸时,操作的注意事项是_______________________________。
(2)步骤③中,为了使反应在50~60℃下进行,常用的方法是___________________________________。
(3)步骤④中洗涤粗硝基苯应使用的仪器是___________________________________________________。
(4)步骤④中粗产品用5%![]() 溶液洗涤的目的是___________________________________________。
溶液洗涤的目的是___________________________________________。
(5)纯硝基苯是无色、密度比水_______________________________(填“小”或“大”)的油状液体,它具有________味。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是![]()
A.常温下可用铁制容器来盛装浓硫酸、说明常温下铁与浓硫酸不反应
B.同一元素的各种同位素的物理性质不同、化学性质相同
C.金属元素的原子只有还原性,离子只有氧化性
D.取碘水于试管中,加入汽油振荡后静置,其现象为下层呈紫红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种化合物,有的是药物,有的是香料。它们的结构简式如图所示:

(1)化合物A的分子式是___;A中含有的官能团的名称是___。
(2)A、B、C、D四种化合物中互为同分异构体的是___。(填序号)
(3)化合物B的核磁共振氢谱中出现___组峰。
(4)1molD最多能与___mol的氢气发生加成反应;1molD与足量Br2水混合,最多能和___ molBr2发生反应
(5)已知C的一种同分异构体满足:①能够发生水解反应;②能够发生银镜反应;③能够使FeCl3溶液显紫色;④苯环上的一氯代物有2种。请写出它的结构简式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷(As)是第四周期ⅤA族元素,可以形成As2O3、As2O5、H3AsO3、H3AsO4等化合物,有着广泛的用途。回答下列问题:
(1)画出砷的原子结构示意图____________。
(2)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式________。该反应需要在加压下进行,原因是________。
(3)已知:As(s)+![]() H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+![]() O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH2
2As(s)+![]() O2(g) =As2O5(s) ΔH3
O2(g) =As2O5(s) ΔH3
则反应As2O5(s) +3H2O(l)= 2H3AsO4(s)的ΔH =_________。
(4)298 K时,将20 mL 3x mol·L1 Na3AsO3、20 mL 3x mol·L1 I2和20 mL NaOH溶液混合,发生反应:AsO33(aq)+I2(aq)+2OH![]() AsO43(aq)+2I(aq)+ H2O(l)。溶液中c(AsO43)与反应时间(t)的关系如图所示。
AsO43(aq)+2I(aq)+ H2O(l)。溶液中c(AsO43)与反应时间(t)的关系如图所示。

①下列可判断反应达到平衡的是__________(填标号)。
a.溶液的pH不再变化
b.v(I)=2v(AsO33)
c. c (AsO43)/c (AsO33)不再变化
d. c(I)=y mol·L1
②tm时,v正_____ v逆(填“大于”“小于”或“等于”)。
③tm时v逆_____ tn时v逆(填“大于”“小于”或“等于”),理由是_____________。
④若平衡时溶液的pH=14,则该反应的平衡常数K为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A.用铜作电极电解硫酸铜溶液: 2Cu2+ + 2H2O ![]() 2Cu+ O2↑+4H+
2Cu+ O2↑+4H+
B.用银氨溶液检验乙醛中的醛基: CH3CHO+2Ag(NH3)2++2OH-![]() CH3COO-+NH4++3NH3+2Ag↓+H2O
CH3COO-+NH4++3NH3+2Ag↓+H2O
C.苯酚钠溶液中通入少量的CO2: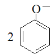 +H2O
+H2O![]()
![]() +CO32-
+CO32-
D.氢氧燃料电池的负极反应式:O2 + 2H2O + 4e-= 4OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com