
【题目】利用钛白工业的副产品FeSO4(含Al2(SO4)3和少量重金属离子)可以生产电池级高纯超微细草酸亚铁。其工艺流程如下:

已知:①5Fe2++ MnO4-+8H+=5Fe3++Mn2++4H2O
5C2O42-+2MnO4-+16H+=10CO2↑+2Mn2++8H2O
(1)沉淀过程的反应温度为40℃,温度不宜过高的原因除了控制沉淀的粒径外,还有 。
(2)滤液经处理可得到副产品 。
(3)实验室测定高纯超微细草酸亚铁组成的步骤依次为:
步骤1:准确称量一定量草酸亚铁样品,加入25 mL 2 mol·L-1的H2SO4溶解。
步骤2:用0.2000 mol·L-1标准KMnO4溶液滴定,消耗其体积30.40 mL。
步骤3:向滴定后的溶液中加入2 g Zn粉和5 mL 2 mol·L-1的H2SO4溶液,将Fe3+还原为Fe2+。
步骤4:过滤,滤液用上述标准KMnO4溶液滴定,消耗溶液10.00 mL。
则样品中C2O42-的物质的量为 。(写出计算过程)
(4)将一定量高锰酸钾溶液与酸化的草酸亚铁溶液混合,测得反应 液中Mn2+的浓度随反应时间t的变化如图,其变化趋势的原因可能为 。

【答案】(1)NH3H2O受热易分解,挥发出NH3,Fe(OH)2受热易分解。(2分)
(2)(NH4)2SO4(2分)
(3)解:由题意知,C2O42-消耗KMnO4溶液体积为(30.40-10.00)=20.4mL,
5C2O42-+2MnO4-+16H+=10CO2↑+2Mn2++8H2O
5 2
n 20.4×10-3×0.2000mol
解得 n=0.0102mol (4分)
(4)生成的Mn2+作催化剂,随着Mn2+浓度增加,反应速率越来越快。(2分)
【解析】试题分析:(1)温度不宜过高的原因除了控制沉淀的粒径外,还有NH3H2O受热易分解,挥发出NH3,Fe(OH)2受热易分解
(2)沉淀步骤中加入一水合氨,生成氢氧化亚铁沉淀的同时还有硫酸铵生成,所以副产品是(NH4)2SO4
(3)由题意知氧化C2O42-和Fe2+共消耗0.2000 mol·L-1标准KMnO4溶液体积30.40 mL,步骤3、4标准KMnO4溶液只氧化Fe2+消耗KMnO4溶液体积10.00mL,所以C2O42-消耗KMnO4溶液体积为(30.40-10.00)=20.4mL,由5C2O42-+2MnO4-+16H+=10CO2↑+2Mn2++8H2O得5C2O42-~2MnO4-,所以C2O42-的物质的量为20.4×10-3×0.2000×5/2=0.0102mol;
(4)从图像上观察,随着反应对进行,曲线的斜率越来越大,说明单位时间内Mn2+的浓度越来越大,所以反应速率越来越快,反应中若温度不变,只能是生成的Mn2+作催化剂,随着Mn2+浓度增加,反应速率越来越快。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】在己经发现的一百多种元素中,除稀有气体外,非金属元素只有十多种但与生产生活有密切的联
系。
(1)为了提高煤的利用率,常将其气化为可燃性气体,主要反应是碳和水蒸气反应生成水煤气,化学反应方程式为_________________。
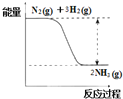
(2)氮是动植物生长不可缺少的元素,合成氨的反应对人类解决粮食问题贡献巨大,反应如下:N2(g)+3H2(g) ![]() 2NH3(g)
2NH3(g)
①合成氨的反应中的能量变化如图所示.该反应是__________反应 (填“吸热”或“放热”),其原因是反应物化学键断裂吸收的总能量__________(填“大于”或“小于”)生成物化学键形成放出的总能量。
②在一定条件下,将一定量的N2和H2的混合气体充入某密闭容器中,一段时间后,下列叙述能说明该反应达到平衡状态的是_____________(填序号)。
A. 容器中混合气体的密度不随时间变化 B. 断裂3molH-H键的同时断裂6molN-H键
C.N2、H2、NH3的物质的量之比为1:3:2 D.容器中的压强不随时间变化
(3)键性电池具有容量大、放电电流大的特点,固而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s)
则该电池的负极反应是_________,放电时,外电路中每通过0.2mol电子,锌的质量理论上减小______。
查看答案和解析>>
科目:高中化学 来源: 题型:
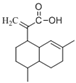
【题目】有机物X可作为合成青蒿素的一种基本原料,已知X的结构如下,下列有关X的说法正确的是
 ( )
( )
A. X为烃的含氧衍生物
B. X最多可以和3mol H2发生加成反应
C. X只能发生取代反应和加成反应
D. X可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且褪色原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除去有关物质中杂质的方案中,正确的是( )
选项 | 物质(括号内为杂质) | 除去杂质使用的试剂 | 除去杂质的方法 |
A | Cl2气(HCl气) | NaOH溶液,浓硫酸 | 洗气 |
B | NH4Cl溶液(FeCl3) | NaOH溶液 | 过滤 |
C | Na2CO3固体(NaHCO3) | Ba(OH)2溶液 | 过滤 |
D | I2 (H2O) | CCl4 | 萃取、分液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以淀粉为主要原料合成-种具有果香味的物质C和化合物d的合成路线如下图所示。回答下列问题:

(1)B分子中的官能团名称为_______________。
(2)反应⑧的反应类型为_______________。
(3)反应③的化学方程式为_________________。反应⑤的化学方程式为___________________。
(4)反应⑥用于实验室制乙烯,为除去其中可能混有的SO2应选用的试剂是_______________。
(5)己知D的相对分子量为118,其中碳、氢两元素的质量分数分别为40.68%、5.08%,其余为氧元素,则D能发生酯化反应,且分子中只有两种不同化学环境的氢,则D的结构简式______________。
(6)请补充完整检验反应①淀粉水解程度的实验方案:取反应①的溶液2mL于试管中,_____________。
实验中可供选择的试剂:10%的NaOH溶液、新制Cu(OH)2悬浊液、碘水.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法错误的是
A. 1 LpH=1 Ba(OH)2溶液中所含OH-的数目为0.2NA
B. 28g聚乙烯![]() 中含有的碳原子数为2NA
中含有的碳原子数为2NA
C. 1 mol CH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-的数目为NA
D. 1 mol Na与O2完全反应生成Na2O和Na2O2的混合物,转移的电子总数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaHCO3在潮湿的空气中会缓慢分解,Na2CO3会吸收空气中的水分:Na2CO3+nH2O=Na2CO3·nH2O(n为平均值,n≤10)。取没有妥善保管已部分变质的一定质量的NaHCO3样品溶于水配成溶液,慢慢滴入稀盐酸并不停地搅拌,加入盐酸的体积与生成的CO2的体积(标准状况)如下表。(不计溶于水的CO2气体)

试求:
(1)该盐酸溶液的物质的量浓度为_______mol·L-1。
(2)未变质前NaHCO3的物质的量为 ________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,容器内某反应中M、N的物质的量随反应时间变化的曲线如下图,下列表述中正确的是

A. t3时,正反应速率大于逆反应速率
B. t2时,正逆反应速率相等,反应达到平衡状态
C. 化学方程式为:2M= N
D. t1时,N的浓度是M浓度的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
①将金属Na投入水中:2Na+2H2O=2Na++2OH-+H2↑
②在硫酸溶液中加入氢氧化钡溶液至中性:Ba2++OH-+H++SO2-4=BaSO4↓+H2O
③碳酸氢钠溶液中滴加盐酸:HCO3-+H+=CO2↑+H2O
④氢氧化钠中滴加醋酸:OH-+H+=H2O
A. ①③④ B. ①③ C. ②④ D. ①②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com