
��ѧ����ʵ��Ϊ������ѧ�ƣ������й�ʵ���������ȷ����
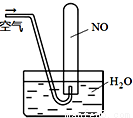
A������֧�ֱ�װ��̼���ƺ�̼�����ƹ�����Թ��и��Ӽ���ˮ��ǰ���¶Ƚ��ͣ������¶�����
B����100mL����ƿ�м���4.0gNaOH���壬Ȼ���ˮ���̶��ߣ�����1.0mol/L��NaOH��Һ
C���������ظ������Һ�м�NaOH����Һ��ɫ�ɳ�ɫ������Ϊ��ɫ
D����ͼ��ʾ�����ſ�����ͨ�룬�Թ���Һ�������������������֧�Թܣ�����Һ�����½���
C
��������
���������A����̼���ƺ�̼�����ƹ�����μ�����ˮ������̼������ˮ��Ӧ����̼���ƾ��壬��Ӧ���ȣ���̼������ֻ����ˮ�⣬ˮ�ⷴӦΪ���ȷ�Ӧ���¶Ƚ��ͣ�A����B������ƿ��������һ�������Ũ����Һ����������ϡ�ͻ��ܽ���壬B����C�������������ƣ�������Ũ�Ƚ��ͣ�ʹ��ƽ��Cr2O72-���Ⱥ�ɫ��+H2O 2H++2CrO42-����ɫ���������ƶ�����Һ��Ϊ��ɫ��C��ȷ��D�������к��е���������������ˮ�����ˮ���ܳ��������Թܣ�D����ѡC��
2H++2CrO42-����ɫ���������ƶ�����Һ��Ϊ��ɫ��C��ȷ��D�������к��е���������������ˮ�����ˮ���ܳ��������Թܣ�D����ѡC��
���㣺���黯ѧʵ��������������ж�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ�����и�����ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧ�Ѿ�������������ĸ������棬����˵����ȷ����
A���ߴ��ȵĹ赥�ʹ㷺�����������ά�����ά��ǿ��ᡰ��·��
B�����Ĺ̶�ֻ���ڸ��¡���ѹ�������������²���ʵ��
C�����ø����������ҩ�ý��һ�����彡���������Σ��
D��������أ�K2FeO4����һ�����͡���Ч�����ˮ������������ɱ���������ܾ�ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ӱ�ʡ�����и���12��������ѧ�Ծ��������棩 ���ͣ�ѡ����
��������˳����ȷ����
�����ȶ��ԣ�HF�� H2O��NH3
�����Ӱ뾶��Na+��Mg2+��F-
�����ʵ��۵㣺ʯӢ��ʳ�Σ���
�ܽ������������OH-��C6H5O-�� HCO3-
�ݷ�ɢϵ�з�ɢ�����ӵ�ֱ����Fe��OH��3����Һ��Fe��OH��3���壾FeCl3��Һ
A���٢ۢ� B���٢ۢܢ� C���ڢ� D��ȫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��㶫ʡ�����и�����ѧ���������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ˮ��Һ�У��ܴ��������һ��������
A��Na+��H+��NO3����SO32�� B��K+��H+��SO42����CH3COO��
C��Mg2+��NH4+��SO42����Cl�� D��K+��Fe3+��Cl����SCN��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ����11���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��������������Һ�д����������
A��Na+��NH4+��CO32����Br�� B��Fe2+��H+��ClO����Cl��
C��Al3+��Ca2+��HCO3����SO42�� D��Fe3+��Cu2+��NO3����OH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���㽭ʡ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ������
�������������������������Ҫԭ��֮һ���������������ж��ַ�����
��1������ClO2�����������ﷴӦ�������£�
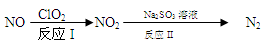
��ӦI�ķ���ʽ��2NO+ClO2+H2O == NO2+HNO3+HCl���÷�Ӧ����������Ϊ ��
��ӦII�Ļ�ѧ����ʽΪ ��
��2�����ü������ԭ���������֪��
CH4(g) + 4NO2(g) === 4 NO(g) + CO2(g) + 2H2O(g) ��H1
CH4(g) + 4NO(g) === 2 N2(g) + CO2(g) + 2H2O(g) ��H2
����֪NO�����ֽ�ΪNO2�����N2���壬д���÷�Ӧ���Ȼ�ѧ����ʽ ��
������һ��NO��NO2�Ļ�����壬��ƽ����Է�����Ϊ34����16g�����������ԭ�û���� �壬ǡ����ȫ��Ӧ���ɵ�����������̼�����ˮ���������ų�����1042.8kJ����û��������NO��NO2�����ʵ���֮��Ϊ ������֪������Ӧ��H2= ��1160 kJ��mol-1����H1= ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���㽭ʡ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��Na2SO3��Һ�������Ṥҵβ���еĶ����������û��Һ���е��ѭ�������������¹��ս�����ѭ�������������������ӽ���Ĥ���ѭ������������ͼ��ʾ��������˵���д������
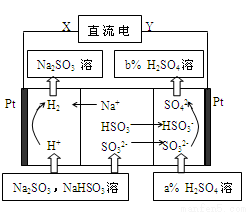
A��XΪֱ����Դ�ĸ�����YΪֱ����Դ������
B��ͼ�������������������b��a
C���ù����еIJ�Ʒ��ҪΪH2SO4��H2
D��������pH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���㽭ʡ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A������Ӽ䷢������ײ������Ч��ײ
B������Ӧ��Ũ�Ȼ�ӿ췴Ӧ���ʣ�ԭ���������˻���Ӱٷ������Ӷ�ʹ��Ч��ײ��������
C�����ȷ�Ӧ�������¶ȣ�v������v���С
D�����������ķ�Ӧ�ﵽƽ�������ѹǿ��ƽ����ܲ��ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���㽭ʡ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ������
��12�֣���֪ij��Ӧ�ڲ�ͬ�����µķ�Ӧ���̿��Ա�ʾ����ͼ��
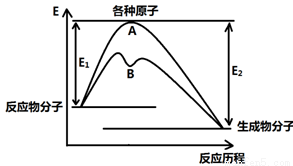
E1��ʾ��Ӧ����ӱ��ԭ�������յ�������E2��ʾ��Щԭ�����³ɼ��γ�������ų�����������ش��������⣺
��1����ͼ�жϸ÷�Ӧ�� ��������š����ȷ�Ӧ����÷�Ӧ���棬����ﵽƽ��������������䣬�����¶ȣ���Ӧ���ת���� �����������С�����䡱��������B���̱����˷�Ӧ�ı������Ϊ ������ĸ����
A������Ӧ���Ũ�� B�������¶� C������ѹǿ D��ʹ�ô���
��2���±�������һЩ��ѧ���ļ��ܣ�
��ѧ�� | H��H | Cl��Cl | O=O | O��H | H��Cl |
���ܣ�kJ��mol-1�� | 436 | 247 | x | 463 | 431 |
����ͼ�б�ʾ��ӦH2(g) +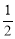 O2(g)=H2O(g) ��H= - 241.8 kJ��mol-1����x= kJ��mol-1������һλС������
O2(g)=H2O(g) ��H= - 241.8 kJ��mol-1����x= kJ��mol-1������һλС������
�ڴ��������������¿����������Ȼ������巴Ӧ�û���������ͬʱ������һ����̬����������ϱ�����д�����Ȼ�ѧ����ʽ �����÷�Ӧ����1 mol���ӷ���ת��ʱ��ͼ��������A��E1= kJ������һλС������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com