
19世纪门捷列夫的突出贡献是
| A.提出了原子学说 | B.提出了分子学说 |
| C.发现了稀有气体 | D.发现了元素周期律 |
科目:高中化学 来源: 题型:单选题
下图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是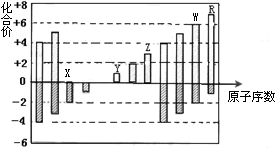
| A.原子半径:Z>Y>X |
| B.气态氢化物的还原性:W>R |
| C.WX3和水反应形成的化合物是离子化合物 |
| D.含Z的盐溶液一定显示酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述中错误的是( )
| A.原子半径:Na>Si>Cl | B.稳定性:SiH4<HCl<H2S |
| C.金属性:Na>Mg>Al | D.酸性:H3PO4<H2SO4<HClO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法中正确的是
A.所有主族元素正化合价数,等于它的族序数
B.ⅦA族元素的原子随核电荷数的增加,得电子能力逐渐减弱
C.前三周期元素中共有非金属元素12种
D.ⅠA、ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知短周期元素的离子aA2+、bB+、cC3-、dD- 都具有相同的电子层结构,则下列叙述正确的是
| A.原子半径A>B>D>C | B.原子序数 d > c > b > a |
| C.离子半径C>D>B>A | D.单质的还原性A>B>D>C |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素X、Y、Z的原子序数依次增大,Y为ⅠA族元素,X与Z同主族,3种元素原子的最外层电子数之和为13,下列判断正确的是( )
| A.Y元素位于第2周期 | B.Y、Z均能与X形成不只一种化合物 |
| C.X是VA族元素 | D.氢化物的稳定性:HnZ > HnX |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
W、X、Y、Z、R属于短周期元素。已知它们都不是稀有气体元素,W的原子半径是所属周期中最大,X元素的原子最外层电子数为m,次外层电子数为n,Y元素的原子L层电子数为m+n,M层电子数m-n,Z元素与Y元素同主族,R元素原子与X元素原子的核外电子数之比为2∶1。下列叙述中,错误的是
| A.分别由Y、Z组成的单质一定都为原子晶体 |
| B.W与X形成的两种化合物中阴、阳离子的个数比均为1∶2 |
| C.Y、Z、R最高价氧化物对应水化物的酸性强弱顺序:R>Z>Y |
| D.X的氢化物比R的氢化物稳定,X的氢化物熔沸点比R的氢化物低 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )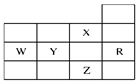
| A.W元素最高价含氧酸酸性强于Y元素最高价含氧酸酸性 |
| B.Z的阴离子电子层结构与R原子的相同 |
| C.p能级未成对电子数最多的是Z元素 |
| D.X元素是电负性最大的元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列排列顺序不正确的是
| A.熔点:Al>K>Na | B.微粒的半径:Cl- >Na+>Mg2+>Al3+ |
| C.热稳定性:HF>HCl>HBr>HI | D.结合质子能力:AlO-2>CO32->F- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com