
为探讨化学平衡移动原理与氧化还原反应规律的联系,某同学通过改变浓度研究“2Fe3++2I- 2Fe2++I2”反应中Fe3+和Fe2+的相互转化。实验如下:
2Fe2++I2”反应中Fe3+和Fe2+的相互转化。实验如下:
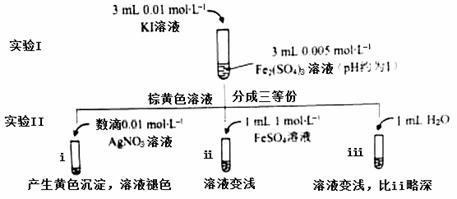
(1)待实验I溶液颜色不再改变时,再进行实验II,目的是使实验I的反应达到 。
(2)iii是ii的对比试验,目的是排除有ii中 造成的影响。
(3)i和ii的颜色变化表明平衡逆向移动,Fe2+向Fe3+转化。用化学平衡移动原理解释原因: 。
(4)根据氧化还原反应的规律,该同学推测i中Fe2+向Fe3+转化的原因:外加Ag+使c(I-)降低,导致I-的还原性弱于Fe2+,用右图装置(a、b均为石墨电极)进行实验验证。

①K闭合时,指针向右偏转,b作 极。
②当指针归零(反应达到平衡)后,向U型管左管滴加0.01 mol/L AgNO3溶液,产生的现象证实了其推测,该现象是 。
(5)按照(4)的原理,该同学用上图装置进行实验,证实了ii中Fe2+向Fe3+转化的原因,
①转化原因是 。
②与(4)实验对比,不同的操作是 。
(6)实验I中,还原性:I->Fe2+;而实验II中,还原性:Fe2+>I-,将(3)和(4)、(5)作对比,得出的结论是 。
【答案】
(1)化学平衡状态(2)溶液稀释对颜色变化
(3)加入Ag+发生反应:Ag++I-=AgI↓,c(I-)降低;或增大c(Fe2+)平衡均逆向移动
(4)①正 ②左管产生黄色沉淀,指针向左偏转。
(5)①Fe2+随浓度增大,还原性增强 ,使Fe2+还原性强于I-
②向U型管右管中滴加1mol/L FeSO4溶液。
(6)该反应为可逆氧化还原反应,在平衡时,通过改变物质的浓度,可以改变物质的氧化、还原能力,并影响平衡移动方向
 【考点定位】考查化学平衡、电化学、以及化学实验设计等知识
【考点定位】考查化学平衡、电化学、以及化学实验设计等知识
【名师点晴】本题以“2Fe3++2I- 2Fe2++I2”反应中Fe3+和Fe2+的相互转化为基本素材,考查化学平衡状态的判断、平衡的移动、原电池原理、化学实验设计等内容,要求学生在解答本题时能充分接受、吸收、整合所给信息,分析和解决化学问题,同时本题第(2)(5)等小问也体现了对化学实验与科学探究能力的考查。题目难度不是很大。解答本题时还要注意答题的规范性。
2Fe2++I2”反应中Fe3+和Fe2+的相互转化为基本素材,考查化学平衡状态的判断、平衡的移动、原电池原理、化学实验设计等内容,要求学生在解答本题时能充分接受、吸收、整合所给信息,分析和解决化学问题,同时本题第(2)(5)等小问也体现了对化学实验与科学探究能力的考查。题目难度不是很大。解答本题时还要注意答题的规范性。


科目:高中化学 来源: 题型:
下列各组物质互为同系物的是
A. C6H5OH和C6H5CH2OH B. CH3OH和HOCH2CH2OH
C. HCOOH和C17H35COOH D. CH3Cl和CH2Cl2
查看答案和解析>>
科目:高中化学 来源: 题型:
贝诺酯是由阿斯匹林、扑热息痛经化学拼合制备的解热镇痛抗炎药,其合成反应式(反应条件略去)如下:
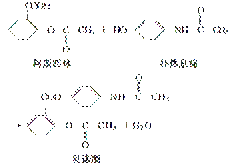
下列叙述错误的是( )
A.FeCl3溶液可区别阿斯匹林和扑热息痛
B.1 mol阿斯匹林最多可消耗2 mol NaOH
C.常温下贝诺酯在水中的溶解度小于扑热息痛
D.C6H7NO是扑热息痛发生类似酯水解反应的产物
查看答案和解析>>
科目:高中化学 来源: 题型:
 ⑴右图是部分主族元素第一电离能梯度图,图中,a点对应的元素为氢,
⑴右图是部分主族元素第一电离能梯度图,图中,a点对应的元素为氢,
b、c两点对应的元素分别为 、 (填元素符号)。
⑵将CrCl3·6H2O溶解在适量水中得到深绿色溶液,溶液中Cr3+以
[Cr(H2O)5Cl]2+形式存在。
①上述溶液中,不存在的微粒间作用力是 (填标号)。
A.离子键 B.共价键 C.金属键 D.配位键 E.范德华力
②[Cr(H2O)5Cl]2+中Cr3+的轨道杂化方式不是sp3,理由是 。
 ⑶下面关于晶体的说法不正确的是________。
⑶下面关于晶体的说法不正确的是________。
A.晶体熔点由低到高:CF4<CCl4<CBr4<CI4
B.硬度由大到小:金刚石>碳化硅>晶体硅
C.熔点由高到低:Na>Mg>Al
D.晶格能由大到小:NaF> NaCl> NaBr>NaI
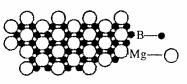
⑷硼化镁晶体在39K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,右图是该晶体微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为 。
⑸铁的金属密堆积方式为体心立方结构,结构如图所示。

则晶胞中铁原子的配位数为______。若铁原子的半径为r pm,写出该堆积方式的空间利用率的表达式(不要求算出结果)_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某模拟"人工树叶”电化学实验装置如右图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O)。下列说法正确的是( )
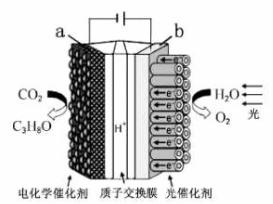
A.该装置将化学能转化为光能和电能
B.该装置工作时,H+从b极区向a极区迁移
C.每生成1 mol O2,有44 g CO2被还原
D.a电极的反应为:3CO2 + 16H+-18e-= C3H8O+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是碳粉,MnO2,ZnCl2和NH4Cl等组成的糊状填充物,该电池在放电过程产生MnOOH,回收处理该废电池可得到多种化工原料,有关数据下表所示:
溶解度/(g/100g水)
|
化合物 | 0 | 20 | 40 | 60 | 80 | 100 |
| NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
| ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 |
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-39 |
回答下列问题:
(1)该电池的正极反应式为 ,电池反应的离子方程式为:
(2)维持电流强度为0.5A,电池工作五分钟,理论上消耗Zn g。(已经F=96500C/mol)
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有ZnCl2和NH4Cl,二者可通过____分离回收;滤渣的主要成分是MnO2、______和 ,欲从中得到较纯的MnO2,最简便的方法是 ,其原理是 。
(4)用废电池的锌皮制备ZnSO4·7H2O的过程中,需去除少量杂质铁,其方法是:加稀硫酸和H2O2溶解,铁变为_____,加碱调节至pH为 时,铁刚好完全沉淀(离子浓度小于1×10-5mol/L时,即可认为该离子沉淀完全);继续加碱调节至pH为_____时,锌开始沉淀(假定Zn2+浓度为0.1mol/L)。若上述过程不加H2O2后果是 ,原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
用一种试剂可鉴别乙醛、乙酸、乙醇3种物质,这种试剂是----------------------------( )
A、金属钠 B、新制Cu(OH)2 C、水 D、紫色石蕊试液
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物A的结构简式如下, 下列有关A的性质叙述中,错误的是: -----------( )
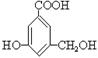 A.A与金属钠完全反应时,两者物质的量之比为1:3
A.A与金属钠完全反应时,两者物质的量之比为1:3
B.A与氢氧化钠完全反应时,两者物质的量之比为1:3
C.A能与碳酸钠溶液反应
D.A既能与羧酸反应,又能与醇反应
查看答案和解析>>
科目:高中化学 来源: 题型:
某气态烃含C 85.7%,含H 14.3%,在标准状况下的密度是2.5g/L。该烃能使酸性高锰酸钾溶液或溴水褪色。求该烃的分子式,并写出它的各种同分异构体的结构简式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com