
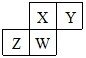 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法错误的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法错误的是( )| A. | 原子半径:Z>W>X>Y | |
| B. | 元素X、Y、Z、W的最高化合价分别与其主族序数相等 | |
| C. | 最简单气态氢化物的热稳定性:Y>X>W>Z | |
| D. | 最高价氧化物对应水化物的酸性:X>W>Z |
分析 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,结合元素周期表结构可知,X、Y应该位于第二周期、Z、W位于第三周期;W原子的质子数是其最外层电子数的三倍,设W的最外层电子数为x,则3x=2+8+x,解得:x=5,W为P元素,则Z为Si元素、X为N元素、Y为O元素,据此结合元素周期律知识解得.
解答 解:短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,结合元素周期表结构可知,X、Y应该位于第二周期、Z、W位于第三周期;W原子的质子数是其最外层电子数的三倍,设W的最外层电子数为x,则3x=2+8+x,解得:x=5,W为P元素,则Z为Si元素、X为N元素、Y为O元素,
A.X、Y含有两个电子层,核电荷数Y大于X,则原子半径X>Y;Z、W含有3个电子层,核电荷数W的解答,其原子半径较小,则原子半径大小为:Z>W>X>Y,故A正确;
B.Y为氧元素,氧元素没有最高正价,故B错误;
C.最简单气态氢化物的热稳定性取决于非金属性大小,非金属性:Y>X>W>Z,则其最简单氢化物稳定性大小为:Y>X>W>Z,故C正确;
D.再根据氧化物对应水合物的酸性与非金属性大小有关,非金属性X>W>Z,则再根据含氧酸的酸性大小为:X>W>Z,故D正确;
故选B.
点评 本题考查了原子结构与元素周期律的关系,题目难度中等,明确原子结构与元素周期表的关系为解答关键,注意熟练掌握元素周期律的内容,试题培养了学生的分析能力及灵活应用能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 湿润的蓝色石蕊试纸遇氨气变红 | |
| B. | 实验室制备氨气的试剂和装置可为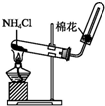 | |
| C. | 蘸有浓氨水的玻璃棒和蘸有浓硝酸的玻璃棒相靠近,两棒之间会产生大量的白烟 | |
| D. | 用氨气做喷泉实验,都会形成红色喷泉 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所含分子数相等 | B. | 分子间的平均距离相等 | ||
| C. | 分子中的电子总数相等 | D. | 氧原子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 min | B. | 3 min | C. | 4 min | D. | 5 min |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L中含有4 g NaOH的溶液 | |
| B. | 稀释1mL,1mol/L NaOH溶液到1L后所得溶液 | |
| C. | pH=11的溶液 | |
| D. | 0.11 mol/LNaOH溶液跟等体积0.05mol/L H2SO4溶液的混合液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| 目的 | 实验室制O2 | 配置稀硫酸溶液 | 在铁制品上镀铜 | 检查装置气密性 |
| 装置或操作 | 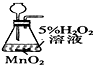 | 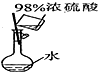 | 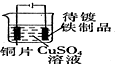 | 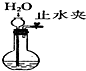 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com