
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| CH4 | CH4O | CH2O | CH2O2 | C2H6 | C2H6O | C2H4O | C2H4O2 |
| A. | ①③④ | B. | ②④⑤ | C. | ②③④ | D. | ②③⑤ |
分析 据表中排布可知,每4个为一组,第一组碳原子为数为1,分别符合通式CnH2n+2、CnH2nO、CnH2nO2、CnH2n+2O,第二组碳原子为数为2,分别符合通式CnH2n+2、CnH2nO、CnH2nO2、CnH2n+2O,所以按此规律排布的第20项是第5组中的第四个,分子式为C5H10O2,然后结合同分异构体解答.
解答 解:据表中排布可知,每4个为一组,第一组碳原子为数为1,分别符合通式CnH2n+2、CnH2nO、CnH2nO2、CnH2n+2O,第二组碳原子为数为2,分别符合通式CnH2n+2、CnH2nO、CnH2nO2、CnH2n+2O,所以按此规律排布的第20项是第5组中的第四个,分子式为C5H10O2,
该物质可能是戊酸及其含有羧基的同系物,可能是酯,可能含有醇羟基和羰基或醛基,
如果是羧酸,一定发生酯化反应,如果含有羧基或羟基,则能和钠反应生成氢气,
故选B.
点评 本题考查探究化学规律,为高频考点,侧重考查学生分析比较总结归纳能力,涉及同分异构体判断、表中分子式规律的判断等知识点,正确判断第20项物质的分子式是解本题关键,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | NaCl发生状态变化时,一定会破坏离子键 | |
| B. | 元素的非金属性越强,单质的活泼性一定越强 | |
| C. | 物质中分子间的作用力越大,分子越稳定 | |
| D. | 只含有共价键的物质一定是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能使溴水褪色的物质一定能和溴水发生加成反应 | |
| B. | 天然蛋白质水解的最终产物是多种α-氨基酸 | |
| C. | 能发生银镜反应的物质都是醛 | |
| D. | 棉花和蚕丝的主要成分都是蛋白质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属铝在生产、生活中得到广泛的应用,主要是因为其可用热还原法冶炼 | |
| B. | 对“地沟油”蒸馏可以获得汽油 | |
| C. | 氯气常用于自来水的消毒,是利用了氯气的强氧化性来杀菌消毒 | |
| D. | 化石燃料使用过程中排放的硫、氮的氧化物是形成酸雨的主要原因 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
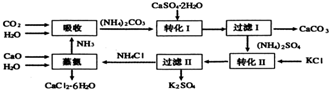
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
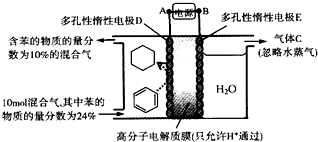
| A. | 多孔性惰性电极E为电解池的阴极 | |
| B. | 装置中气体C为氢气 | |
| C. | 由A至D,导线中电子转移方向为D→A | |
| D. | 装置中阴极的电极反应式为C6H6+6H++6e-═C6H12 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4的摩尔质量是98 g | |
| B. | 1 mol CO2的体积是22.4 L | |
| C. | 0.2 mol H2O的质量是3.6 g | |
| D. | 0.1 mol/LFeCl3溶液中,C1-的物质的量浓度为0.1 mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com