
【题目】在某容积一定的密闭容器中,可逆反应:A(g)+B(g)xC(g),符合下列图象(Ⅰ)所示关系.由此推断对图(Ⅱ)的正确说法是( ) 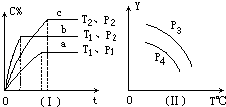
A.p3>p4 , Y轴表示A的质量
B.p3>p4 , Y轴表示混合气体平均摩尔质量
C.p3>p4 , Y轴表示混合气体密度
D.p3<p4 , Y轴表示B的百分含量
【答案】AD
【解析】解答:解:由图(1)可知,压强为P2时,温度T1先到达平衡,故温度T1>T2 , 且温度越高,平衡时C的质量分数越低,故升高温度平衡向逆反应移动,正反应为放热反应;温度为T1时,压强P2先到达平衡,故压强P2>P1 , 且压强越大,平衡时C的质量分数越高,故增大压强平衡向正反应移动,正反应为体积减小的反应,故x=1,则:
A.如果P3>P4 , 在相同温度下增大压强平衡向正反应方向移动,则A的转化率增大,A质量减小,同时升高温度平衡向逆反应方向移动,A的转化率降低,A质量增大,图象与实际不符合,故A错误;
B.C.混合气体的总质量不变,容器的体积不变,混合气体的密度不变,故C错误;
D.P3<P4 , 增大压强,平衡向正反应移动,B的含量减小,同时升高温度平衡向逆反应方向移动,B的含量应增大,图象与实际不符,故B错误;
P3>P4 , 增大压强,平衡向正反应移动,混合气体总的物质的量减小,混合气体的总质量不变,平均相对分子质量增大,温度升高平衡向逆反应移动,混合气体总的物质的量增大,平均相对分子质量减小,图象与实际相符,故D正确;
故选AD.


 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:
【题目】电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:①电解池中X极上的电极反应式为;在X极附近观察到的现象是 .
②Y电极上的电极反应式为;检验该电极反应产物的方法是 .
(2)如用电解方法精炼粗铜,电解液a选用CuSO4溶液,则①X电极的材料是 , 电极反应式为 .
②Y电极的材料是 , 电极反应式为 . (说明:杂质发生的电极反应不必写出)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3.52 克铜镁合金完全溶解于50mL、密度为1.400g/cm3、质量分数为63%的浓硝酸中,得到NO2气体3584mL(标准状况),向反应后的溶液中加入适量的1.0mo1/LNaOH溶液,恰使溶液中的金属离子全部沉淀。下列说法不正确的是
A. 合金中铜和镁的物质的量相等
B. 加入NaOH溶液的体积是100mL
C. 得到的金属氢氧化物的沉淀为6.24 克
D. 浓硝酸与合金反应中起氧化性的硝酸的物质的量为0.16 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多沙唑嗪盐酸盐是一种用于治疗高血压的药物。多沙唑嗪的合成路线如下:

(1) A分子结构中在一个面上最多有________个原子。D→E 发生的化学反应类型是_______。 D 中含有的官能团名称是________。
(2)B→C的化学方程式是______. (K2CO3 在方程式中作催化剂)
(3)满足下列条件①和②的D的同分异构体的个数为________。
写出一种同时满足下列条件①②③的同分异构体的结构简式_________。
①苯的衍生物,且苯环上只有两种处于对位的取代基
②分子结构中含羧基,且该物质能发生银镜反应
③水解后的产物才能与FeCl3溶液发生显色反应
(4)E→F的反应中还可能生成一种有机副产物,该副产物的结构简式为________。
(5)由F制备多沙唑嗪的反应中要加入试剂X (C10H10N3O2Cl),X的结构简式为 ________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水综合利用要符合可持续发展的原则,其联合工业体系(部分)如图所示,
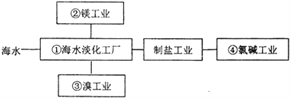
下列说法不正确的是
A. ①中可采用反渗透膜法,该法用到的半透膜可用于渗析操作
B. ②中工业上要制金属镁,可通过电解饱和氯化镁溶液的方法来获取
C. ③中提溴需要对含溴溶液加有机溶剂进行富集,该操作称为萃取
D. ④中氯碱工业电解饱和食盐水,采用的是阳离子交换膜法进行电解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.增大反应物浓度,可增大单位体积内活化分子的百分数
B.对于有气体参加的化学反应,若增大压强,可增大活化分子的百分数
C.升高温度,可以增大活化分子百分数
D.活化分子间的碰撞一定是有效碰撞
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合物锂离子电池是以Li+嵌入化合物为正、负极的二次电池。如图为一种聚合物锂离子电池示意图,其工作原理为LiNiO2+6C![]() Li1-xNiO2+LixC6,下列说法错误的是
Li1-xNiO2+LixC6,下列说法错误的是

A. 该电池充电可能引起电池正极发生金属锂沉积
B. 充电时当外电路通过1mole-时理论上由2molLi0.9C6转化为Li0.4C6
C. 电池放电时电解质的微粒Li+由负极向正极移动
D. 电池放电时正极的电极反应式为Li1-xNiO2+xLi++xe-=LiNiO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂废水中含游离态氮,通过下列实验测定其浓度
①取水样10.0mL于锥形瓶,加入10.0mLKI溶液(足量),滴入指示剂2﹣3滴.
②取一滴定管依次用自来水,蒸馏水洗净,然后注入0.01molL﹣1的Na2S2O3溶液,调整液面,记下读数.
③将锥形瓶置于滴定管下进行滴定,发生的反应为:I2+2Na2S2O3=2NaI+Na2S4O6 .
试回答下列问题:
(1)步骤①加入的指示剂是 .
(2)步骤②应使用式滴定管.
(3)试描述滴定终点的现象: .
(4)若耗去Na2S2O3溶液20.00mL,则废水中C12的物质的量浓度为 .
(5)请指出实验中的一处明显错误: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com