
【题目】下列能用勒夏特列原理解释的是( )
A. 铁在潮湿的空气中易腐蚀
B. H2、I2、HI平衡混和气加压后颜色变深
C. 往往需要在催化剂条件下SO2氧化成SO3
D. 棕红色NO2加压后颜色先变深后变浅
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】下列电离方程式中正确的是( )
A.Al2(SO4)3=2Al3++3SO42﹣
B.Na2SO4=Na++SO42﹣
C.Ca(NO3)2=Ca2++2(NO3)2﹣
D.Ba(OH)2=Ba2++OH2﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(NOCl)是有机合成中的重要试剂。回答下列问题:
(1)NOCl虽然不稳定,但其原子均达到8e-稳定结构,NOCl的电子式为_________________。
(2)一定条件下,在密闭容器中发生反应:2NOCl(g)![]() 2NO(g)+Cl2(g),其正反应速率表达式为v正=k·cn( NOCl)(k为速率常数),测得v正和c(NOCl)的关系如表:
2NO(g)+Cl2(g),其正反应速率表达式为v正=k·cn( NOCl)(k为速率常数),测得v正和c(NOCl)的关系如表:
序号 | c(NOCl)/(mol·L-1) | v正/(mol·L-1·s-1) |
① | 0.30 | 3.60×10-9 |
② | 0.60 | 1.44×10-8 |
则n=_________;k=___________。
(3)25 ℃时,制备亚硝酰氯所涉及的热化学方程式和平衡常数如表:
序号 | 热化学方程式 | 平衡常数 |
① | 2NO2(g)+NaCl(s) | K1 |
② | 4NO2(g)+2NaCl(s) | K2 |
③ | 2NO(g)+Cl2(g) | K3 |
则该温度下,ΔH3=______kJ/mol;K3=______(用K1和K2表示)。
(4)25℃时,在体积为2L的恒容密闭容器中通入0.08 mol NO和0.04 molCl2发生上述反应③,若反应开始与结束时温度相同,数字压强仪显示反应过程中压强(p)随时间(t)的变化如图曲线a所示,则ΔH3=______(填“>”“<”或“=”)0;若其他条件相同,仅改变某一条件,测得其压强(p)随时间(t)
的变化如图曲线b所示,则改变的条件是_____________;K3=___________L/mol;在5 min时,再充入0.08 mol NO和0.04 molCl2,则混合气体的平均相对分子质量将_____________(填“增大”、“减小”或“不变”)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外小组用如图装置制取溴苯,并证明反应为取代反应。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
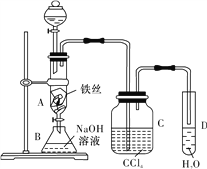
(1)观察到A中的现象是________________,D中导管口可观察到的现象是________________。
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是__________________________。
(3)C中盛放CCl4的作用是________________。
(4)若要证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入________溶液,若观察到________________,即能证明。
(5)将锥形瓶中液体分液,得到的溴苯中仍含有杂质________及少量水分,用固体无水硫酸钠等作吸水剂可除去水分,另一种杂质的除去方法是________________(已知溴苯不溶于水,密度大于水,沸点156 ℃)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各溶液中一定能大量共存的离子组是( )
A. 使酚酞溶液呈红色的溶液中:Mg2+、Cu2+、SO![]() 、K+
、K+
B. 使pH试纸呈红色的溶液中:Fe2+、K+、NO![]() 、Cl-
、Cl-
C. c(H+)=10-14 mol·L-1溶液中:Na+、AlO![]() 、S2-、SO
、S2-、SO![]()
D. 水电离出的c(H+)为10-12mol·L-1的溶液中:K+、Na+、CO![]() 、Ca2+
、Ca2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物A含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现如图所示的物质之间的变化:

回答下列问题:
(1)写出所含物质的化学式:固体B_____,沉淀D_____。
(2)写出①、④两个反应的化学方程式:
①_______________________________________
④_______________________________________
(3)写出②、③两个反应的离子方程式:
②_______________________________________
③_____________________________________
(4)设计实验检验溶液F中所含溶质的阳离子:___________________________。
(5)分别写出Al2O3和Fe2O3在工业上的一种主要用途:
Al2O3︰_____________________________________
Fe2O3︰_____________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA,实验室制备联氨(N2H4)的化学方程式为:2NH3 +NaClO=N2H4 +NaCl+ H2O。下列说法正确的是
A. 0. lmolN2H4中所含质子数为1. 8NA
B. 0. 1mol·L-1的NaClO溶液中,ClO-的数量为0.1NA
C. 消耗4.48LNH3时,转移电子数为0.2NA
D. 1.6g N2H4中存在共价键总数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属的描述正确的是( )
A.金属都是银白色、都有金属光泽,能导电、导热,有延展性
B.含金属元素的离子一定都是阳离子
C.钠和钾的合金可用作原子反应堆的导热剂
D.金属原子失电子越多,其还原性越强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com