
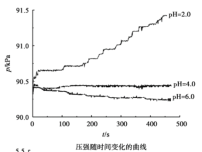
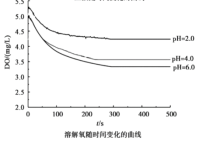
【题目】用如图所示装置及试剂进行铁的电化学腐蚀实验探究,测定具支锥形瓶中压强随时间变化关系以及溶解氧随时间变化关系的曲线如下。

下列说法不正确的是
A.压强增大主要是因为产生了H2
B.整个过程中,负极电极反应式为:Fe–2e- = Fe2+
C.pH= 4.0时,不发生析氢腐蚀,只发生吸氧腐蚀
D.pH= 2.0时,正极电极反应式为:2H+ + 2e- = H2↑ 和 O2 + 4e- + 4H+ = 2H2O
【答案】C
【解析】
Fe在酸性环境下会发生析氢腐蚀,产生氢气;若介质的酸性很弱或呈中性,并且有氧气参与,此时Fe就会发生吸氧腐蚀,吸收氧气。
A.pH=2.0的溶液,酸性较强,因此锥形瓶中的Fe粉能发生析氢腐蚀;析氢腐蚀产生氢气,因此会导致锥形瓶内压强增大,A项正确;
B.锥形瓶中的Fe粉和C粉以及酸溶液构成了原电池,Fe粉作为原电池的负极;由于溶液均为酸性,所以发生的电极反应式为:![]() ,B项正确;
,B项正确;
C.若pH=4.0时只发生吸氧腐蚀,那么锥形瓶内的压强会有下降;而图中pH=4.0时,锥形瓶内的压强几乎不变,说明除了吸氧腐蚀,Fe粉还发生了析氢腐蚀;消耗氧气的同时也产生了氢气,因此锥形瓶内压强几乎不变,C项错误;
D.由图可知,pH=2.0时,锥形瓶内的溶解氧减少,说明有消耗氧气的吸氧腐蚀发生;同时锥形瓶内的气压增大,说明有产生氢气的析氢腐蚀发生;因此,正极反应式有:![]() 和
和![]() ,D项正确;
,D项正确;
答案选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.甲烷的一氯取代物只有 1 种结构,说明甲烷是正四面体结构而不是平面结构
B.乙醇与金属钠能反应,在相同条件下比水与金属钠的反应缓慢
C.![]() 分子中的 4 个碳原子位于同一平面内
分子中的 4 个碳原子位于同一平面内
D.在酒精灯上加热铜片后插入乙醇,会生成有刺激性气味的物质,反应结束后铜片质量与加热前相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。

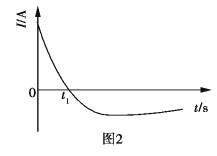
下列说法错误的是( )
A.0~t1时,原电池的负极是Al片
B.0~t1时,正极的电极反应式是![]() +2H++e=NO2↑+H2O
+2H++e=NO2↑+H2O
C.t1后,原电池的正、负极发生互变
D.t1后,正极上每得到0.3mol电子,则负极质量减少2.7g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实的方程式不正确的是
A.用明矾作净水剂:Al3+ + 3H2O![]() Al(OH)3(胶体)+ 3H+
Al(OH)3(胶体)+ 3H+
B.NO2球浸泡在冷水中,颜色变浅: 2NO2(g) ![]() N2O4(g) ΔH< 0
N2O4(g) ΔH< 0
C.用醋酸除去水垢:2H++CaCO3 = Ca2++CO2↑+H2O
D.CO2通入苯酚钠溶液中出现浑浊:![]() +CO2+H2O→
+CO2+H2O→![]() +NaHCO3
+NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】维纶(聚乙烯醇缩甲醛纤维)可用于生产服装、绳索等。其合成路线如下:
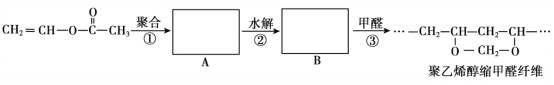
下列说法不正确的是
A.反应①是加聚反应
B.高分子A的链节中只含有一种官能团
C.通过质谱法测定高分子B的平均相对分子质量,可得其聚合度
D.反应③的化学方程式为:![]() +nHCHO→
+nHCHO→![]() +(2n-1)H2O
+(2n-1)H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“空气吹出法”海水提溴的工艺流程如图:
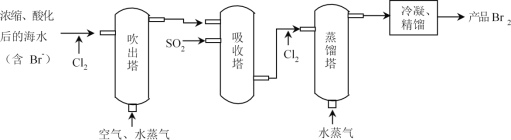
下列说法正确的是( )
A.从吹出塔进入吸收塔的物质只有Br2
B.从吸收塔流出的溶液主要含HBr和H2SO4
C.两次通入水蒸气的作用都是参加反应
D.第一次通入Cl2的目的是氧化Br-,第二次通Cl2的目的是氧化SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用系统命名法 命名下列有机物
(1)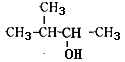 ____________________________________________, 由 该 物 质 制 得 烯 烃 的 反 应 条 件 为_____,
____________________________________________, 由 该 物 质 制 得 烯 烃 的 反 应 条 件 为_____,
(2)![]() _____,由该物质生成顺式聚合物的结构简式是_____。
_____,由该物质生成顺式聚合物的结构简式是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化氢分解制取氢气和硫磺的反应原理为2H2S(g)![]() S2(g)+2H2(g),在2.0 L恒温恒容密闭容器中充入2.0 mol H2S,反应过程中的部分数据如下表所示:
S2(g)+2H2(g),在2.0 L恒温恒容密闭容器中充入2.0 mol H2S,反应过程中的部分数据如下表所示:
n/mol t/min | n(H2S) | n(S2) | n(H2) |
0 | 2.0 | 0 | 0 |
2 | 1.0 | ||
4 | 0.8 | ||
6 | 0.6 |
下列说法不正确的是( )
A.0~2min 生成H2的平均反应速率为0.25 mol·L-1·min-1
B.上述反应的平衡常数K=0.675
C.3分钟时,H2S的分解率一定小于60%
D.平衡后,向容器中通入少量O2,平衡正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在25℃时,FeS、CuS的溶度积常数(Ksp)分别为6.3×10-18、1.3×10-36。常温时下列有关说法正确的是
A. 向H2S的饱和溶液中通入少量SO2气体溶液的酸性增强
B. 将足量的CuSO4溶解在0.1 mol/L的H2S溶液中,溶液中Cu2+的最大浓度为1.3×10-35mol/L
C. 因为H2SO4是强酸,所以反应:CuSO4十H2S=CuS↓+H2SO4不能发生
D. 除去工业废水中的Cu2+可以选用FeS作沉淀剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com