
 )的路线如图所示:
)的路线如图所示:
 ,A和甲醇发生酯化反应生成邻羟基苯甲酸甲酯B
,A和甲醇发生酯化反应生成邻羟基苯甲酸甲酯B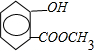 ,邻羟基苯甲酸甲酯和硝酸发生取代反应生成含有硝基、酚羟基和酯基的C,C和铁、HCl发生还有反应生成D,所以D的结构简式为:
,邻羟基苯甲酸甲酯和硝酸发生取代反应生成含有硝基、酚羟基和酯基的C,C和铁、HCl发生还有反应生成D,所以D的结构简式为: ,C的结构简式为
,C的结构简式为 ,B的结构简式为
,B的结构简式为 ,据此解答.
,据此解答. ,苯环上即可与Br2发生取代反应,也可与H发生加成反应,酚羟基和氨基都易被氧化,不能发生消去反应,故选:c;
,苯环上即可与Br2发生取代反应,也可与H发生加成反应,酚羟基和氨基都易被氧化,不能发生消去反应,故选:c; ,
, ;
; ,符合a、苯环上有2个取代基,且能发生水解反应和银镜反应;b.1mol该物质与足量的Na反应生成0.5mol H2条件的其同分异构体的结构有:
,符合a、苯环上有2个取代基,且能发生水解反应和银镜反应;b.1mol该物质与足量的Na反应生成0.5mol H2条件的其同分异构体的结构有: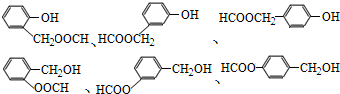 共6种,故答案为:6;
共6种,故答案为:6; .
.


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案科目:高中化学 来源: 题型:



查看答案和解析>>
科目:高中化学 来源: 题型:
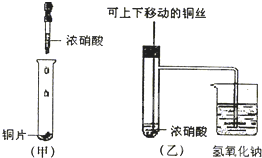 Ⅰ甲同学向品红溶液中通入一种气体后,品红褪色.乙同学设计了一个很简单的实验便知甲同学通的是Cl2还是SO2.他的实验方案是
Ⅰ甲同学向品红溶液中通入一种气体后,品红褪色.乙同学设计了一个很简单的实验便知甲同学通的是Cl2还是SO2.他的实验方案是
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com