
(10分)A、B、C、D、E、F为短周期主族元素,原子序数依次增大,A是相对原子质量最小的元素;D的+1价阳离子与氖原子具有相同的电子层结构;C和E同主族,C和E的原子序数之和是A和D的原子序数之和的2倍;B和C为同周期元素,B的最高价氧化物对应的水化物是一种强酸。请根据以上信息回答下列问题。
(1)F元素在元素周期表中的位置是______________。
(2)B的氢化物的水溶液呈碱性,用离子方程式表示原因:______________。
(3)A2C2可以制备C2,该反应的化学方程式是______________。
(4)A、B、C 三种元素形成的既含离子键又含共价键的化合物的化学式是___________。
(5)E的单质和E的最高价含氧酸的浓溶液加热发生反应,该反应的化学方程式是______________。
(1)第三周期VIIA族;(2)NH3·H2O NH4++OH-;(3)2H2O2
NH4++OH-;(3)2H2O2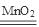 2H2O+O2↑;(4)NH4NO3
2H2O+O2↑;(4)NH4NO3
(5)S+2H2SO4(浓) 3SO2↑+2H2O
3SO2↑+2H2O
解析试题分析:根据题意可推知:A是H;B是N;C是O;D是Na;E是S;F是Cl。(1)F元素在元素周期表中的位置是第三周期VIIA族;(2)B的氢化物的水溶液呈碱性的原因是NH3·H2O NH4++OH-;(3)H2CO2在MnO2作催化剂时发生分解反应可以制备O2,该反应的化学方程式是2H2O2
NH4++OH-;(3)H2CO2在MnO2作催化剂时发生分解反应可以制备O2,该反应的化学方程式是2H2O2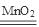 2H2O+O2↑;(4)A、B、C 三种元素形成的既含离子键又含共价键的化合物的化学式是NH4NO3。(5)E的单质和E的最高价含氧酸的浓溶液加热发生反应,该反应的化学方程式是S+2H2SO4(浓)
2H2O+O2↑;(4)A、B、C 三种元素形成的既含离子键又含共价键的化合物的化学式是NH4NO3。(5)E的单质和E的最高价含氧酸的浓溶液加热发生反应,该反应的化学方程式是S+2H2SO4(浓) 3SO2↑+2H2O。
3SO2↑+2H2O。
考点:考查元素的推断、元素在周期表中中的位置、物质的性质、化学方程式、电离方程式的书写的知识。


科目:高中化学 来源: 题型:单选题
短周期元素X,Y,Z在周期表中的位置如图所示,则下列说法中错误的是( )
| | | X |
| | Y | |
| Z | | |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族。下列叙述正确的是( )
| A.原子半径的大小顺序: Y<Z<W<X |
| B.化合物YX、ZX2、WX3中化学键的类型相同 |
| C.非金属性的强弱顺序:X>W>Z |
| D.元素W的最高价氧化物对应水化物的酸性比Z的弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(每空1分,共6分)
A、B、C、D、E、F为六种短周期主族元素,它们的原子序数依次增大;A元素的原子半径最小;B元素原子的最外层电子数是次外层电子数的3倍;C与A同主族,且与E同周期;E元素的最外层电子数是次外层电子数的0.75倍,D既可与C的最高价氧化物的水化物反应,也可与E的最高价氧化物的水化物反应,均有A元素的单质生成。
请回答下列问题:
(1)写出F元素原子结构示意图 ,元素B在周期表中的位置 。
(2)判断C、D、E原子半径的大小顺序 (填写元素符号,下同),比较B和E的气态氢化物的稳定性大小 。
(3)写出单质D与C的最高价氧化物的水化物反应的离子方程式 。
(4)由A、B、C、E四种元素共同构成的两种化合物在溶液中相互间可发生化学反应,试写出该反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(12分,每空1分)下表是元素周期表的一部分,回答下列有关问题: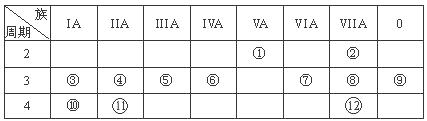
(1)写出下列元素符号:① ,⑥ ,⑦ 。
(2)画出原子的结构示意图:④ ,⑧ 。
(3)在①~?元素中,金属性最强的元素是 ,非金属性最强的元素是 ,最不活泼的元素是 。(均填元素符号)
(4)元素⑦与元素⑧相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 。
a.常温下⑦的单质和⑧的单质状态不同 b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(5)第三周期中原子半径最大的元素是 (用元素符号表示),跟它同周期的ⅦA元素是 (用元素符号表示)
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(6分)A、B、C三种元素的原子具有相同的电子层数,而B的核电荷数比A大1,C原子的电子总数比B原子的电子总数多4; 1molA的单质跟足量盐酸反应,可置换出标准状况下22.4L的H2,这时A转变为与氖原子具有相同电子层结构的离子。请回答:
(1)用电子式表示A和C组成的化合物的形成过程为______________________;
(2)B离子的电子式是 ,与B的离子具有相同电子数的分子中,有一种分子
可与盐酸化合生成盐,该分子的电子式是 ;
周期表中与C上下相邻的同族元素形成的气态氢化物中,沸点最高的是 ,(填
氢化物化学式),原因是 ;
写出B最高价氧化物的水化物和C最高价氧化物的水化物之间反应的离子方程式(本
题涉及的含C元素的物质均易溶于水): 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了①~⑨九种元素在周期表中的位置。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | | | | ⑤ | | ⑥ | | |
| 3 | ① | ③ | ④ | | | | ⑦ | ⑨ |
| 4 | ② | | | | | | ⑧ | |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(9分)下图为周期表中的一部分。已知A、B、C、D均为短周期元素,
A与D原子序数之和为C原子序数的1.5倍。
(1)B元素符号是: _______、D在元素周期表中第_______族。
(2)四种元素中原子半径最大的是(填元素符号)_______,B、C、D三种离子中半径最大的是(填离子符号)_______。
(3)B比C的氢化物的沸点高是因为_____ __;A、D两元素的气态氢化物相互反应的生成物的电子式: ,其中存在_______键、_______(填“极性”或“非极性”)共价键。
(4)写一个离子方程式证明C和D的非金属性相对强弱: 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(14分)A、B、C、D、E、F六种短周期元素,其原子序数依次增大,其中B与C同周期,D与E和F同周期,A与D同主族,C与F同主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的主族元素。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。
请回答下列问题。
(1)元素D在周期表中的位置 。
(2)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示) 。
(3)若E是非金属元素,其单质在电子工业中有重要应用,请写出其氧化物溶于强碱溶液的离子方程式: 。
(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出反应的化学方程式: 。冶炼金属E时,用石墨做电极。E在(填“阴”或“阳”) 极得到,电解过程中,阳极石墨需要不断补充,结合电极反应说明其原因是 。
(5)由A、B、C三种元素以原子个数比4:2:3形成化合物X,X中所含化学键类型有 。土壤中含有X中的阳离子在硝化细菌的催化作用下被氧气氧化为其阴离子,写出其离子方程式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com