
化合物Bilirubin在一定波长的光照射下发生分解反应,反应物浓度随反应时间变化如图所示,计算反应4~8 min间的平均反应速率和推测反应16 min时反应物的浓度,结果应是( )

A.2.5 μmol·L-1·min-1和2.0 μmol·L-1
B.2.5 μmol·L-1·min-1和2.5 μmol·L-1
C.3.0 μmol·L-1·min-1和3.0 μmol·L-1
D.5.0 μmol·L-1·min-1和3.0 μmol·L-1
科目:高中化学 来源: 题型:
化学反应中的能量变化,是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同所致。下图为N2(g)和O2(g)生成NO(g)过程中的能量变化:

(1)人们通常把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,则N≡N键的键能为____________kJ·mol-1。根据上图写出N2(g)和O2(g)生成NO(g)的热化学方程式:
________________________________________________________________________。
(2)NO(g)分解生成N2(g)和O2(g)的热化学方程式为________________;当有16 g O2(g)生成时,该反应中放出的热量为________kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
新型纳米材料氧缺位铁酸盐(MFe2Ox,3<x<4,M=Mn、Zn、Ni,且均为+2价,下同)是由铁酸盐MFe2O4经过高温反应得到的。
(1)将纳米材料氧缺位铁酸盐分散在蒸馏水中,所形成的分散系属于__________。
(2)MFe2O4中Fe元素的化合价为______________。
(3)铁酸盐MFe2O4经过高温反应得到MFe2Ox的反应属于__________(填“氧化还原”或“非氧化还原”)反应。
(4)在酸性条件下,Fe2O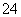 容易转化为Fe2+,某反应体系中共存在下列6种粒子:Fe2O
容易转化为Fe2+,某反应体系中共存在下列6种粒子:Fe2O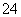 、Fe2+、H+、H2O、Cu2O、Cu2+,则该反应中的氧化剂是________,还原剂是________。
、Fe2+、H+、H2O、Cu2O、Cu2+,则该反应中的氧化剂是________,还原剂是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A、B可发生反应:4A(g)+5B(g)===4C(g)+6D(g)(g代表气态)。在2 L密闭容器中加入4 mol A和5 mol B,若经5 s后,剩下的A是2 mol,则B的反应速率是( )
A.0.25 mol·(L·s)-1 B.0.2 mol·(L·s)-1
C.0.225 mol·(L·s)-1 D.0.15 mol·(L·s)-1
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列事实中,什么因素影响了化学反应的速率。
(1)集气瓶中,H2和Cl2的混合气体,在瓶外点燃镁条时发生爆炸________。
(2)等质量的大理石块和大理石粉分别与相同浓度的盐酸反应,大理石粉反应快______________________________________。
(3)硫在空气中燃烧发出微弱的淡蓝色火焰,在纯氧中迅速燃烧发出明亮的蓝紫色火焰__________________________。
(4)熔化的KClO3放出气泡很慢,撒入少量MnO2产生气体很快____________。
(5)同浓度、同体积的盐酸中放入同样大小的锌条和镁条,产生气体有快有慢______________________________________。
(6)夏天的食品易霉变,冬天就不易发生该现象___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
等体积等物质的量浓度的MOH强碱溶液和HA弱酸溶液混合后,混合溶液中有关离子浓度关系正确的是( )
A.c(M+)>c(OH-)>c(A-)>c(H+)
B.c(M+)>c(A-)>c(H+)>c(OH-)
C.c(M+)>c(A-)>c(OH-)>c(H+)
D.c(M+)+c(H+)>c(A-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,pH=12的一元弱碱和pH=1的一元强酸等体积混合后(不考虑混合后溶液体积的变化),恰好完全反应,则下列说法正确的是( )
A.反应后的溶液呈酸性
B.弱碱的浓度小于强酸的浓度
C.弱碱中OH-的浓度为0.1 mol·L-1
D.弱碱的浓度大于强酸的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
金属镍有广泛的用途。粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍(已知:氧化性Fe2+<Ni2+<Cu2+),下列叙述正确的是( )
A.阳极发生还原反应,其电极反应式:Ni2++2e-===Ni
B.电解过程中,阳极质量的减少与阴极质量的增加相等
C.电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+
D.电解后,电解槽底部的阳极泥中只有Cu和Pt
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com