
【题目】2SO2(g) +O2(g)=2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99KJ/mol。请回答下列问题:
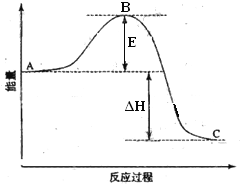
①图中A、C分别表示________、_______;
②E表示________;E的大小对该反应的反应热____(填“有”或“无”)影响。
③该反应通常用V2O5作催化剂,加V2O5会使图△H______(填“变大”、“变小”或“不变”),图中△H =______KJ/mol;
④已知单质硫的燃烧热为296 KJ/mol,计算由S(s)生成3molSO3(g)的△H=________KJ/mol。
【答案】 2mol气态SO2和1mol气态O2所具有的总能量 2mol气态SO3所具有的总能量 活化能 无 不变 -198 KJ/mol -1185 KJ/mol
【解析】(1)①图中A、C分别表示反应物总能量、生成物总能量,故答案为:2mol气态SO2和1mol气态O2所具有的总能量;2mol气态SO3所具有的总能量;
②E为活化能,反应热可表示为生成物总能量能、反应物总能量的大小之差,活化能的大小与反应热无关,故答案为:活化能;无;
③催化剂能够降低反应的活化能,加V2O5会使图中B点降低,因为催化剂可以降低反应的活化能,但不能改变反应物的总能量和生成物的总能量之差,即不改变反应热,因1mol SO2(g)氧化为1mol SO3的△H=-99kJmol-1,所以2molSO2(g)氧化为2molSO3的△H=2×(-99kJmol-1)=-198kJmol-1,故答案为:不变; -198 kJmol-1;
④因单质硫的燃烧热为296kJmol-1,则①:S(s)+O2(g)=SO2(g)△H=-296kJmol-1,而 1mol SO2(g)氧化为1mol SO3的△H=-99kJmol-1,则②:SO2(g)+![]() O2(g)=SO3(g)△H=-99kJmol-1,则根据盖斯定律,①×3+②×3可得:S(s)+
O2(g)=SO3(g)△H=-99kJmol-1,则根据盖斯定律,①×3+②×3可得:S(s)+![]() O2(g)=SO3(g),△H=3×[(-296kJmol-1)+(-99kJmol-1)]=-1185 KJmol-1,故答案为:-1185 KJmol-1。
O2(g)=SO3(g),△H=3×[(-296kJmol-1)+(-99kJmol-1)]=-1185 KJmol-1,故答案为:-1185 KJmol-1。


科目:高中化学 来源: 题型:
【题目】(1)如图所示装置中,两玻璃管及烧杯中是滴有酚酞的NaCl饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极。

①接通S1后,C(Ⅰ)附近溶液变红,两玻璃管中均有气体生成。则电极C(Ⅰ)是_____极(填“阳”或“阴”);C(Ⅱ)电极反应所得气体产物为_____________。
②通电一段时间后(玻璃管中液面未脱离电极), 断开S1,接通S2,电流表的指针发生偏转,此时电极C(Ⅰ)为____(填“正”或“负”)极;C(Ⅰ)的电极反应为______。
(2)若用此装置精炼粗铜,断开S2接通S1电解液选用CuSO4溶液;粗铜接电池的_______(填“正”或“负”)极,阴极发生的电极反应为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 利用高纯度硅制造的太阳能电池板可将光能直接转化为电能
B. 胶体的本质特征是丁达尔效应
C. 食品包装袋中常放入小袋的生石灰,目的是防止食品氧化变质
D. 宋·王希孟《千里江山图》卷中的绿色颜料铜绿的主要成分是氢氧化铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种金属,当A、B组成原电池时,电子流动方向A →B ;当A、D组成原电池时,A为正极;B与E构成原电池时,电极反应式为:E2++2e-=E,B-2e-=B2+则A、B、D、E金属性由强到弱的顺序为( )
A. A﹥B﹥E﹥D B. A﹥B﹥D﹥E
C. D﹥A﹥B﹥E D. D﹥E﹥A﹥B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用下列图Ⅰ装置进行铜跟浓硫酸反应等一系列实验。
请回答:

(1)图I装置中的收集装置B应连接图Ⅱ中的__________(填“a”或“b”)进口。
(2)用此装置制SO2与将铜片直接加入试管A加热反应相比,其优点主要是______________。
(3)下列叙述中,描述正确的是______________。
A.A试管中发生了Cu与浓硫酸的反应,其中浓硫酸只体现了强氧化性
B.熄灭酒精灯后,因为A试管中的玻璃导管存在,整套装置不易发生倒吸
C.C试管中的紫色石蕊试液会变红,是因为二氧化硫溶于水后生成了 H2SO3
D.D、E试管中品红和高锰酸钾溶液都会褪色,其褪色原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用含少量镁粉的铝粉制取纯净的氢氧化铝,下述操作步骤中最恰当的组合是①加盐酸溶解;②加烧碱溶液溶解;③过滤;④通入过量CO2生成Al(OH)3沉淀;⑤加入盐酸生成Al(OH)3沉淀;⑥加入过量烧碱溶液。
A. ①⑥⑤③ B. ②③⑤③ C. ②③④③ D. ①③⑤③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型纳米材料MFe2Ox (3<x<4)中M表示+2价的金属元素,在反应中化合价不发生变化。常温下,MFe2Ox能使工业废气中的SO2转化为S,流程如下,则下列判断正确的是( )
![]()
A.MFe2Ox是氧化剂
B.SO2是该反应的催化剂
C.x<y
D.MFe2Oy是还原产物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com