
【题目】能源危机当前是一个全球性问题,“开源节流”是应对能源危机的重要举措。
(1)下列做法有助于能源“开源节流”的是__(填字母)。
A.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
B.大力开采煤、石油和天然气以满足人们日益增长的能源需求
C.开发太阳能、水能、风能、地热能等新能源,不使用煤、石油等化石燃料
D.减少资源消耗,增加资源的重复使用、资源的循环再生
(2)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示。
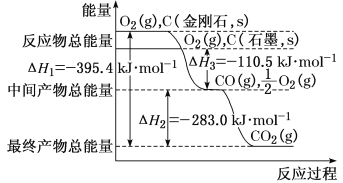
①在通常状况下,金刚石和石墨相比较,__(填“金刚石”或“石墨”)更稳定,石墨的燃烧热为ΔH=___。
②12g石墨在一定量空气中燃烧,生成气体36g,该过程放出的热量为__kJ。
(3)已知:N2、O2分子中化学键的键能分别是946kJ·mol-1、497kJ·mol-1。N2(g)+O2(g)=2NO(g)ΔH=+180.0kJ·mol-1。NO分子中化学键的键能为__。
(4)综合上述有关信息,请写出用CO除去NO的热化学方程式:__。
【答案】AD 石墨 -393.5kJ·mol-1 252.0 631.5kJ·mol-1 2NO(g)+2CO(g)=N2(g)+2CO2(g) ΔH=-746.0kJ·mol-1
【解析】
(2)①物质能量越高,物质越不稳定;燃烧热是指1mol物质完全燃烧生成稳定的氧化物所释放的能量;
②依据极值计算判断生成的气体组成,再结合热化学方程式计算。
(3)焓变=反应物总键能-生成物总键能;
(4)利用盖斯定律结合已知热化学方程式计算反应热。
(1)只要能减少化石燃料等资源的运用都属于“开源节流”;B.大力开采煤、石油和天然气,不能减少化石燃料的运用,故错误;C.减少使用化石燃料不代表不使用,故错误;A、D能减少化石燃料的运用,故正确,所以选AD。
(2)①图象分析金刚石能量高于石墨,能量越低越稳定,所以说明石墨稳定,根据图象可知1mol石墨完全燃烧生成1mol二氧化碳放出的热量为393.5kJ,则石墨的燃烧热为ΔH=-393.5kJ·mol-1;
②12g石墨物质的量为1mol,在一定量空气中燃烧,依据元素守恒,若生成二氧化碳质量为44g,若生成一氧化碳质量为28g,生成气体36g,28g<36g<44g,所以生成的气体为一氧化碳和二氧化碳气体,设一氧化碳物质的量为x,则二氧化碳物质的量为(1-x)mol,28x+44(1-x)=36g,x=0.5mol,二氧化碳物质的量为0.5mol;根据图像可知生成1molCO2方出的热量为393.5kJ,生成1molCO放出的热量为110.5 kJ,生成二氧化碳和一氧化碳混合气体放出热量=393.5kJmol-1×0.5mol+110.5 kJmol-1×0.5mol=252.0kJ;
(3)焓变=反应物总键能-生成物总键能,设NO分子中化学键的键能为x,则有:946kJmol-1+497kJmol-1-2x=180kJmol-1 得:x=631.5kJmol-1;
(4)已知①C(石墨,s)+O2(g)=CO2(g) △H=-393.5 kJmol-1 ;
②C(石墨,s)+![]() O2(g)=CO(g) △H=-110.5 kJmol-1;
O2(g)=CO(g) △H=-110.5 kJmol-1;
③N2(g)+O2(g)=2NO(g)△H=+180kJmol-1;
由盖斯定律:方程式①×2-②×2-③得 2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=-746.0kJmol-1。


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】某溶液中可能含有H+、![]() 、Mg2+、Al3+、Fe3+、
、Mg2+、Al3+、Fe3+、![]() 、
、![]() 、
、![]() 中的几种。
中的几种。
①若加入锌粒,用排空气法收集到无色无味气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法不正确的是( )
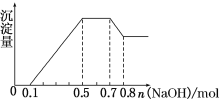
A.溶液中的阳离子有H+、Mg2+、Al3+、![]()
B.溶液中n(Mg2+)=0.1 mol
C.溶液中一定不含![]() 、
、![]() 、Fe3+
、Fe3+
D.n(![]() ∶n(Al3+)∶n(Mg2+)=4∶2∶1
∶n(Al3+)∶n(Mg2+)=4∶2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料。请回答:
(1)基态铜原子的电子排布式为_______________;已知高温下CuO→Cu2O+O2,从铜原子价层电子结构(3d和4s轨道上应填充的电子数)变化角度来看,能生成Cu2O的原因是_________________________。
(2)硒、硅均能与氢元素形成气态氢化物,则它们形成的组成最简单的氢化物中,分子构型分别为____________,若“Si—H”中共用电子对偏向氢元素,氢气与硒反应时单质硒是氧化剂,则硒与硅的电负性相对大小为Se____Si(填“>”、“<”)。
(3)SeO2常温下白色晶体,熔点为340~350℃,315℃时升华,则SeO2固体的晶体类型为_________;若SeO2类似于SO2是V型分子,则Se原子外层轨道的杂化类型为_________。
(4)与镓元素处于同一主族的硼元素具有缺电子性(价电子数少于价层轨道数),其化合物可与具有孤对电子的分子或离子生成配合物,如BF3能与NH3反应生成BF3·NH3。BF3·NH3中B原子的杂化轨道类型为______,B与N之间形成_________键。
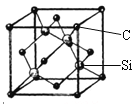
(5)金刚砂(SiC)的硬度为9.5,其晶胞结构如图所示;则金刚砂晶体类型为________,在SiC中,每个C原子周围最近的C原子数目为___个;若晶胞的边长为a pm,则金刚砂的密度表达式为_________g/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁铝合金具有良好的强度、刚性、优良的电磁屏蔽性和导热性,使之成为笔记本电脑和轻薄手机的首选外壳材料。为测定某手机外壳镁铝合金中镁和铝的含最,并回收镁铝,某实验小组设计如下实验方案。
①除去手机外壳的涂层,剪其中一小块,称取其质量;
②组装仪器,检查气密性,用足盘稀盐酸溶解合金;
③测量产生气体的体积,计算结果;
④利用下列流程,从溶解合金后的溶液中回收分离镁铝。
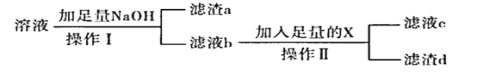
(1)请利用下图给定的仪器组成一套实验装置(每个仪器只能使用一次,可不选用)。各种仪器连接的先后顺序(用小写字母表示)_______

(2)除了测定产生气体的体积外,还应测定_______。
(3)回收流程中,操作I需要的玻璃仪器有烧杯、玻璃棒和_______,为保证回收产品的纯度,操作I后应_______。
(4)滤液b的溶质是_______(填化学式),试剂X是_______。
(5)向滤渣a中加入盐酸,产物是_______(填化学式),若从晶体中获得金属,应进行的操作是_______。
(6)若从除去涂层的手机壳上取样品mg加入足量盐酸后,测得产生的气体nL,实验条件下的气体摩尔体积为VmL/mol,则合金中Mg的质量为________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯吡格雷![]() 是一种血小板凝固抑制剂,其合成路线如图:
是一种血小板凝固抑制剂,其合成路线如图:
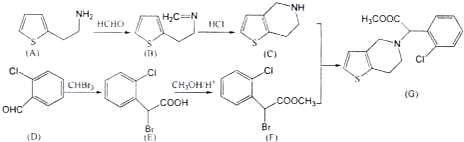
回答下列问题:
![]() 化合物D和F中的含氧官能团分别为 ______ 和 ______
化合物D和F中的含氧官能团分别为 ______ 和 ______ ![]() 填名称
填名称![]() .
.
![]() 有机反应类型:
有机反应类型:![]() : ______ ;
: ______ ;![]() : ______ .
: ______ .
![]() 反应
反应![]() 的化学方程式 ______ .
的化学方程式 ______ .
![]() 化合物
化合物![]()
![]()
![]() 是D的一种同系物,在H的同分异构体中,同时满足下列条件的物质的结构简式为 ______ .
是D的一种同系物,在H的同分异构体中,同时满足下列条件的物质的结构简式为 ______ .
![]() 分子中只含1个环,且有4中不同环境的H;
分子中只含1个环,且有4中不同环境的H;![]() 可与
可与![]() 溶液发生显色反应.
溶液发生显色反应.
![]() 根据已有知识,并结合本题信息,以
根据已有知识,并结合本题信息,以![]() 为起始原料,其他试剂任选,设计制备化合物
为起始原料,其他试剂任选,设计制备化合物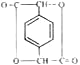 的合成路线图. ______
的合成路线图. ______
合成路线图示例如下:![]() .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温下,固定容积的密闭容器中,有可逆反应2SO3(气) ![]() 2SO2(气)+O2(气),可用来确定该反应已达到平衡状态的是( )
2SO2(气)+O2(气),可用来确定该反应已达到平衡状态的是( )
A.容器内压强不随时间改变B.SO3的消耗速率与SO2的生成速率相等
C.三种气体的分子数比为2:2:1D.容器内混合气体的密度不随时间改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案不能达到实验目的是
实验目的 | 实验方案 | |
A | 证明溴乙烷发生消去反应有乙烯生成 | 向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热,将反产生的气体通入溴的四氯化碳溶液 |
B | 检验卤代烃中卤原子的种类 | 将溴乙烷与氢氧化钠溶液共热,取冷却后反应液,向其中滴加硝酸酸化后的硝酸银溶液 |
C | 检验 | 将 |
D | 验证苯和液溴在 | 将反应产生的混合气体先通入四氯化碳溶液再通入 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t℃时,某一气态平衡体系中含有X、Y、Z、W四种气体物质,此温度下发生反应的平衡常数表达式为:![]() ,有关该平衡体系的说法正确的是( )
,有关该平衡体系的说法正确的是( )
A.升高温度,平衡常数K增大 ,则正反应为吸热反应
B.增大压强,W质量分数增加
C.增大X浓度,平衡向正反应方向移动
D.升高温度,若混合气体的平均相对分子质量变大,则正反应是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一含Ni的单核六配位配合物,其阳离子空间结构为八面体。1mol该配合物的稀水溶液与足量![]() 混合生成
混合生成![]() 沉淀233g;将溶液过滤,滤液与硝酸银溶液混合不生成沉淀。元素分析表明该配合物所含部分原子个数比为
沉淀233g;将溶液过滤,滤液与硝酸银溶液混合不生成沉淀。元素分析表明该配合物所含部分原子个数比为![]() 。
。
(1)请画出Ni的价电子排布图:______________________,H、N、O的电负性由大到小的顺序为______________________。
(2)滤液与硝酸银溶液混合不生成沉淀的原因是___________________________________。
(3)该配合物阴离子的中心原子杂化方式为____________,请写出该配合物的化学式:________________。
(4)多原子分子中各原子若在同一平面,且有相互平行的p轨道,则p电子可以在多个原子间运动,形成“离域![]() 键”。下列微粒中存在“离域
键”。下列微粒中存在“离域![]() 键”的是_________
键”的是_________![]() 填序号
填序号![]() 。
。
A.![]()
![]()
![]()
![]() 苯
苯
(5)如图是六方NiAs晶胞的晶胞图及坐标参数,其中![]() ,
,![]() ,
,![]() 。晶胞顶点、棱上小球为Ni,As在体内。
。晶胞顶点、棱上小球为Ni,As在体内。
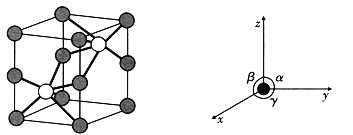
①写出As的配位数为_________,Ni的配位数为_________。
②已知晶胞参数为![]() ,
,![]() ,则晶胞的密度为____________
,则晶胞的密度为____________![]() 写表达式
写表达式![]() 。
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com