


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ΪCu������ΪFe���������ҺΪFeCl3 |
| B������ΪC������ΪFe���������ҺΪFe(NO)3 |
| C������ΪFe������ΪZn���������ҺΪFe2(SO4)3 |
| D������ΪAg������ΪFe���������ҺΪFe2(SO4)3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 Cd+2NiO(OH)+2H2O �ɴ˿�֪���õ�طŵ�ʱ�ĸ��������� �� ��
Cd+2NiO(OH)+2H2O �ɴ˿�֪���õ�طŵ�ʱ�ĸ��������� �� ��| A��Cd(OH)2 | B��Ni(OH)2 | C��Cd | D��NiO(OH) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
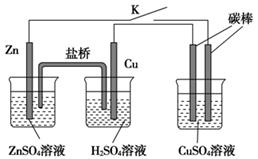
| A��ͭ��Ϊ��������缫��ӦʽΪ��2H����2e��====H2�� |
| B���ձ��Ҳ�̼��Ϊ��������缫�����к�ɫ�������� |
| C����Ӧ������п������Ϊ13 g |
| D��������ͨ�����ӵ����ʵ���Ϊ0.2 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
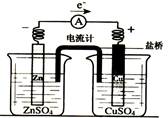
| A��ͭƬ���������ݳ� |
| B��ȡ�����ź�������Ȼ����ƫת |
| C����Ӧ�У������е�K+������CuSO4��Һ |
| D����Ӧǰ��ͭƬ�������ı� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���ڴ�������Ƕп�飬���Լ������屻��ˮ��ʴ������ |
| B����ͭ����ʱ�����Һ�е�c(Cu2��)���ֲ��� |
| C��Na+����ɫ��Ӧ�ʻ�ɫ�����ڻ�ѧ�仯 |
| D���ڵζ�ʵ���У������ü�ʽ�ζ�����ȡ21��0 mL��NaOH��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 Na2Sn������˵������ȷ����
Na2Sn������˵������ȷ����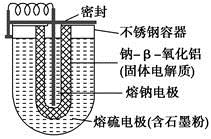
| A������������������ʯī����Ҫ��Ϊ����ǿ������ |
| B���ŵ�ʱNa���������ƶ� |
| C�����ʱ������ӦʽΪ8S��16e��===nS8 |
| D�����ʱ�Ƽ�����ӵ�Դ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
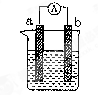
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����ʱ���������Һ�е�H+���ƶ� |
| B������0.4mol����ת�ƣ����ڱ�״��������4.48L���� |
| C����ط�Ӧ�Ļ�ѧ����ʽΪ��CH3CH2OH + O2 = CH3COOH + H2O |
| D�������Ϸ����ķ�ӦΪ��O2 + 4e- + 2H2O = 4OH- |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com