
【题目】甲胺![]() 的性质与氨相似,
的性质与氨相似,![]() 也是一元弱碱,
也是一元弱碱,![]() 时电离常数
时电离常数![]() 。现用
。现用![]() 的稀硫酸滴定
的稀硫酸滴定![]() 的甲胺溶液,溶液中
的甲胺溶液,溶液中![]() 的负对数pOH与所加稀硫酸的体积
的负对数pOH与所加稀硫酸的体积![]() 的关系如图所示,下列说法正确的是( )
的关系如图所示,下列说法正确的是( )
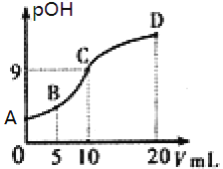
A.B点溶液中存在![]()
B.甲胺在水中的电离方程式为:![]()
C.A、B、C三点溶液中,由水电离出来的![]() :
:![]()
D.C点所在溶液中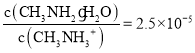
【答案】D
【解析】
A.B点溶液中是反应后得到等浓度的CH3NH2·H2O和CH3NH3+,溶液显碱性说明电离大于离子的水解,溶液中存在c(CH3NH3+)>c(CH3NH2·H2O)>c(OH-)>c(H+),故A错误;
B.CH3NH2·H2O也是一元弱碱,可以电离出氢氧根离子,电离过程为可逆,电离方程式为:CH3NH2·H2O![]() CH3NH3++OH-,故B错误;
CH3NH3++OH-,故B错误;
C.用0.0500mol·L-1的稀硫酸滴定l0mL 0.1000mol·L-1的甲胺溶液滴入10ml恰好完全反应此时生成的是强酸弱碱盐,溶质水解溶液显酸性,促进水的电离,AB点溶液中弱碱过量抑制水的电离,所以A、B、C三点溶液中,水电离出来的c(H+):C>B>A,故C错误;
D.C点所在溶液中pOH=9,氢氧根离子浓度c(OH-)=10-9mol·L-1,![]() =
=![]() ,
,![]() =
=![]() =2.5×10-5,故D正确;
=2.5×10-5,故D正确;
故选:D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】四氯化钛是乙烯聚合催化剂的重要成分,制备反应如下:
①TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)ΔH1=+175.4kJ·mol-1
②C(s)+![]() O2(g)=CO(g)ΔH2=-110.45kJ·mol-1
O2(g)=CO(g)ΔH2=-110.45kJ·mol-1
下列说法正确的是
A.C的燃烧热是-110.45kJ·mol-1
B.若反应①中使用催化剂加快反应速率,单位时间内吸收更多热量,则ΔH1变大
C.反应①中的能量变化如图所示
D.反应TiO2(s)+2Cl2(g)+2C(s)=TiCl4(g)+2CO(g)ΔH=-45.5kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,![]() 的
的![]() 溶液中,
溶液中,![]() 、
、![]() 、
、![]() 三者所占物质的量分数
三者所占物质的量分数![]() 分布系数
分布系数![]() 随pH变化的关系如图所示。下列表述不正确的是
随pH变化的关系如图所示。下列表述不正确的是

A.![]() 的平衡常数
的平衡常数![]()
B.将等物质的量的![]() 、
、![]() 溶于水中,所得溶液pH恰好为
溶于水中,所得溶液pH恰好为![]()
C.常温下HF的电离常数![]() ,将少量
,将少量![]() 溶液加入到足量NaF溶液中,发生的反应为:H2C2O4+F-=HF+HC2O4-
溶液加入到足量NaF溶液中,发生的反应为:H2C2O4+F-=HF+HC2O4-
D.在![]() 溶液中,各离子浓度大小关系为
溶液中,各离子浓度大小关系为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二乙酸—1,4—环己二醇酯可通过下列路线合成:
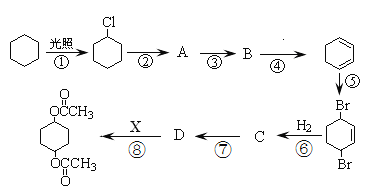
(1)化合物的结构简式:B___;D___。
(2)上述合成过程中没有涉及的反应类型是___。
A.加成 B.消去 C.取代 D.氧化 E.聚合 F.酯化
(3)反应④和反应⑧的反应条件:④___;⑧___。
(4)写出②的反应方程式___;写出⑤的反应方程式___。
(5)请设计合理的方案以CH2=CH—CH=CH2(1,3—丁二烯)和醋酸为原料合成 (用合成路线流程图表示,并注明反应条件)___。
(用合成路线流程图表示,并注明反应条件)___。
提示:①合成过程中无机试剂任选;②合成路线流程图示例如:
CH3CH2OH![]() H2C=CH2
H2C=CH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物的结构可用“键线式”表示,如:CH3CH=CHCH3可简写为![]() ,有机物X的键线式为
,有机物X的键线式为![]() ,下列说法不正确的是( )
,下列说法不正确的是( )
A.X的化学式为C8H10
B.有机物Y是X的同分异构体,且属于芳香烃,则Y的结构简式为![]()
C.X能使酸性高锰酸钾溶液褪色
D.X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某高分子化合物的部分结构如下:是由许多分子中含双键的物质M相互加成而得,下列说法正确的是( )
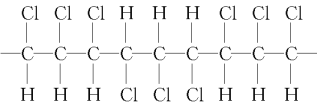
A.该高分子化合物的链节为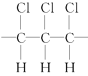
B.该化合物的分子式是C3H3Cl3
C.形成该化合物的单体是CHCl=CHCl
D.该化合物的结构简式可写为CHCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】所有超市、商场、集贸市场等商品零售场所实行塑料购物袋有偿使用制度,一律不得免费提供塑料购物袋。在全国范围内禁止生产、销售、使用厚度小于0.025毫米的塑料购物袋(简称超薄塑料购物袋)。下列说法不正确的是( )
A.在所有超市、商场、集贸市场等商品零售场所实行塑料购物袋有偿使用制度,主要目的是控制塑料制品的使用,减少“白色污染”
B. 的单体是苯乙烯
的单体是苯乙烯
C.聚氯乙烯塑料强度大,抗腐蚀性强,可以用来包装需长时间保存的食品
D.用于食品包装的塑料制品,属于热塑性塑料,可回收再利用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列问题涉及前 20 号元素,请按要求用相应的化学用语作答:
(1)族序数等于周期数 2 倍的元素_____
(2)最外层电子数是内层电子数的一半且单质可作为电极材料的元素, 其在周期表中的位置是_____
(3)原子半径最大的短周期元素和地壳中含量最多的元素形成原子个数比为 1:1 的化合物,其阴离子符号为________________________________
(4)最高正价与最低负价代数和为零的短周期元素,其最高价氧化物与短周期元素中最稳定的气态氢化物的水溶液间发生反应的化学方程式___________________________
(5)第三周期元素中,简单离子半径最小的元素,其离子结构示意图为_____
(6)简单离子 Xn+与 Yn-具有相同的电子层结构,X n+的焰色为淡紫色,则 Y 的最高价氧化物对应水化物的名称为_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在![]() 恒容密闭容器中充入
恒容密闭容器中充入![]() 和
和![]() ,发生反应
,发生反应![]() ,所得实验数据如下表,下列说法正确的是
,所得实验数据如下表,下列说法正确的是 ![]()
![]()
实验编号 | 温度 | 起始时物质的量 | 平衡时物质的量 | ||
|
|
|
| ||
① | 800 |
|
|
|
|
② | 800 |
|
| a | a |
③ | 900 |
|
|
|
|
A.正反应为放热反应
B.实验①中,反应![]() 达平衡,用X表示的平均反应速率
达平衡,用X表示的平均反应速率![]()
C.实验②中,该反应的平衡常数![]()
D.实验②中,达到平衡时,a大于![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com